Sàng lọc hoạt tính gây độc tế bào ung thư của các loài vi tảo và vi khuẩn lam thu tại Nghệ An
Viện Hóa học, Viện Hàn lâm Khoa học và Công nghệ Việt Nam
Số điện thoại: 0984009088; Email: nxnhiem@yahoo.com
Nội dung chính của bài viết
Tóm tắt
Từ các mẫu nước thu mẫu ở 5 thuỷ vực ở khu vực Nghệ An, đã phân lập được 19 chủng vi tảo và vi khuẩn lam. Các mẫu được định danh là Chlorella vulgaris, Aphanizomenon sp., Microcystis aeruginosa, Scenedesmus acuminatus, Anabaena sp., Anabaena circinalis, Microcystis wesenbergii, Nostoc calcicola, Aphanizomenon flos-aquae, Cyclotella sp., Amphora sp., Spirulina platensis, Spirulina maxima, Microcystis sp.XO1, Hapalosiphon welwitschii, Westiellopsis prolifica, Mastigocladus sp., Nostoc sp4. và Nostoc sp5. Các chủng vi tảo được nuôi nhân sinh khối, tạo cao chiết MeOH và sau đó đánh giá tác dụng gây độc tế bào trên các dòng tế bào ung thư phổi (SK-LU-1) và ung thư gan (HepG2). Kết quả cho thấy, có 7/19 mẫu nghiên cứu thể hiện khả năng ức chế trên cả hai dòng tế bào ung thư SK-LU-1 và HepG2 bao gồm Microcystis aeruginosa NA03, Scenedesmus acuminatus NA04,Anabaena sp NA05, A. circinalis NA06,Spirulina platensis NA12, S. maxima NA13và Microcystis sp. NA14 với giá trị IC50 trong khoảng 35 - 95 μg/mL (SK-LU-1) và 42 - 86 μg/mL (HepG2). Đáng chú ý là các mẫu vi tảo Spirulina platensis NA12 và S. maxima NA13và Microcystis sp. NA14 gây độc tế bào mạnh với IC50 trong khoảng từ 35 - 58 μg/mL (SK-LU-1) và 42- 52 μg/mL (HepG2). Nghiên cứu này không chỉ có ý nghĩa đối với việc cung cấp thêm tư liệu về nguồn vi tảo ở Nghệ An, mà còn là cơ sở khoa học để định hướng việc nuôi trồng vi tảo để khai thác, ứng dụng vào phát triển các thuốc có tác dụng chống ung thư.
Abstract
Investigation of the cytotoxic effects of microalgae collected in Nghe An
Freshwater microalgae from Nghe An Province were sampled from five water bodies (Goong Lake, Lam River, Ban Ve Lake, Quynh Luu shrimp ponds, and Vuc Mau Lake). Nineteen axenic strains representing Chlorophyta, Bacillariophyta, and Cyanobacteria were isolated and cultured. Dried biomass was extracted with methanol, and cytotoxicity was evaluated against SK-LU-1 (lung) and HepG2 (liver) cancer cell lines using the SRB assay. Seven of the nineteen extracts showed measurable activity, with IC50 values of 35.0–94.8 μg/mL for SK-LU-1 and 41.9–85.8 μg/mL for HepG2. The most active samples were Spirulina platensis NA12, Spirulina maxima NA13, and Microcystis sp. NA14, which exhibited IC50 values of 35–58 μg/mL (SK-LU-1) and 42–52 μg/mL (HepG2). These results broaden the baseline knowledge of Vietnamese freshwater microalgal chemodiversity and indicate that Spirulina and Microcystis from Nghe An are promising sources of cytotoxic metabolites. Further work shouldofocus on the isolation and structural characterization of the active constituents, and evaluation of their selectivity toward cancer cells.
Từ khóa
Vi tảo, Cyanobacteria, độc tế bào, microalgae, cytotoxicity, Anabaena, Microcystis
Chi tiết bài viết

Bài báo này được cấp phép theo Creative Commons Attribution 4.0 International License.
- Điểm nổi bật:
Nghiên cứu đã thu mẫu, phân lập và định danh 19 mẫu vi tảo/vi khuẩn lam tại Nghệ An.
Dịch chiết methanol của 7/19 mẫu vi tảo/vi khuẩn lam có khả năng ức chế cả hai dòng tế bào ung thư người với giá trị IC50 trong khoảng 35 - 95 μg/mL (dòng tế bào ung thư phổi SK-LU-1) và 42 - 86 μg/mL (dòng tế bào ung thư gan HepG2).
1. ĐẶT VẤN ĐỀ
Vi tảo là các sinh vật quang tự dưỡng và dị dưỡng nhân sơ hoặc nhân thật, có kích thước rất nhỏ, khoảng từ vài µm đến hàng trăm µm. Chúng có cấu trúc tế bào đa dạng, có thể là sinh vật nhân sơ, đơn bào như vi khuẩn lam (Cyanobacteria), đến sinh vật nhân thật, đa bào như tảo xoắn Spirulina, vv. Trong hệ sinh thái, vi tảo có nhiều vai trò quan trọng. Chúng có khả năng chuyển hoá năng lượng mặt trời thành năng lượng hoá học thông qua quá trình quang hợp [1], chúng vừa tạo ra oxy và đóng góp vào quá trình cố định carbon dioxide trong khí quyển của Trái đất, vừa là nguồn thức ăn sống cho nhiều sinh vật thủy sinh, bao gồm động vật phù du, ấu trùng, giáp xác và thân mềm [2]. Vi tảo có phân bố rộng, sống trong nhiều loại môi trường khác nhau (nước ngọt, nước biển, hồ muối, đất, đá, cây cối, trên bề mặt trầm tích v.v.) [1]. Do đó chúng có thể tạo ra các hợp chất hóa học hấp dẫn với cấu trúc mới và các chất có hoạt tính sinh học đa dạng, ví dụ như chống ung thư, kháng viêm, kháng khuẩn, kháng virus, chống đông máu, chống oxy hóa và kháng nấm [3], kích hoạt hệ thống miễn dịch [4], tăng hoạt động của tế bào tiêu diệt tự nhiên (NK cell) [5], và ức chế sự phát triển của tế bào ung thư [6]. Trong thực tiễn, vi tảo trở thành nguồn tài nguyên quan trọng để phát triển thuốc. Một số loài vi tảo như Spirulina, Botryococcus, Chlorella, Dunaliella salna, Haematococcus và Nostoc được nuôi trồng lượng lớn để chiết xuất các hợp chất có hoạt tính sinh học [7, 8].
Do có vai trò quan trọng trong các hệ sinh thái thuỷ sinh, việc thu mẫu và phân lập vi tảo từ các môi trường khác nhau tại Việt Nam là rất cần thiết không chỉ phục vụ cho mục đích khai thác tiềm năng sinh học mà còn là nền tảng cho việc giám sát sinh thái, đánh giá xu hướng chất lượng nước và hiểu rõ sức khỏe cũng như động lực của các hệ sinh thái thủy sinh mà còn để nghiên cứu sâu hơn về đặc điểm sinh học, sinh thái và tiềm năng ứng dụng của chúng. Trên cơ sở đó và cùng với mục tiêu nghiên cứu phát hiện hoạt chất có tác dụng kháng ung thư từ nguồn tài nguyên thiên nhiên Việt Nam, bài báo này thông báo về kết quả thu mẫu, phân lập, định danh các chủng vi tảo từ các hệ sinh thái nước thuộc khu vực Nghệ An và đánh giá tác dụng gây độc tế bào ung thư của các cao chiết từ các loài vi tảo. Kết quả sẽ bổ sung vào danh mục các chủng vi tảo tiềm năng làm tiền đề cho nghiên cứu các hoạt chất sinh học từ vi tảo.
2. VẬT LIỆU VÀ PHƯƠNG PHÁP NGHIÊN CỨU
2.1. Vật liệu
Các mẫu nước chứa mẫu vi tảo được thu tại các sông hồ tại Nghệ An bao gồm 1) hồ Goong (18.6732oN, 105.6959oE; 2) sông Lam (18.9362oN, 105.0861oE); 3) hồ Bản Vẽ (19.3665oN, 104.4998oE); 4) một số ao đầm nuôi tôm (19.1868oN 105.7080oE), và 5) hồ Vực Mấu: (19.2693oN, 105.6325oE) (Hình 1).
*Các dòng tế bào sử dụng trong nghiên cứu: Các dòng tế bào ung thư phổi người (SK-LU-1) và tế bào ung thư gan người (HepG2). Các dòng tế bào do GS. TS. J. M. Pezzuto, Trường Đại học Long-Island, US và GS. Jeanette Maier, trường Đại học Milan, Italia cung cấp.
*Hóa chất, dung môi: ATL III chuẩn (99,0%); nước tinh khiết, ethanol 96% đạt tiêu chuẩn DĐVN V. Môi trường nuôi cấy tế bào: Dulbecco s Modified Eagle Medium (DMEM) hoặc Minimum Esental Medium with Eagle salt (MEME), có bổ sung thêm L-glutamine, sodium pyruvat, NaHCO3, penicillin/streptomycin, 10% FBS (Fetal Bovine Serum), Trypsin-EDTA (0,05%). Các hóa chất cơ bản khác: SRB (Sulforhodamine B), Dimethyl sulfoxide (DMSO), trichloroacetic acid (TCA), Tris base, phosphate buffered saline (PBS), ellipticine, acetic acid. Các hóa chất đều được mua từ hãng Sigma, Hoa kỳ hoặc các công ty khác và đều đạt tiêu chuẩn thí nghiệm.
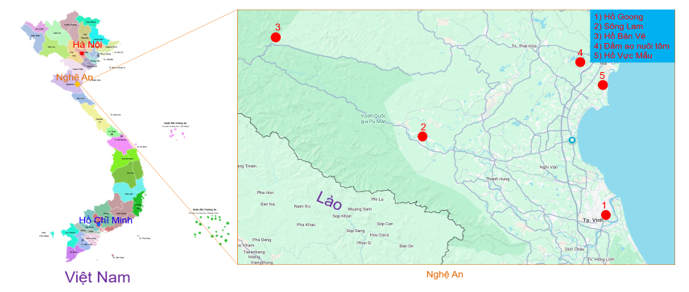
Hình 1. Bản đồ các địa điểm lấy mẫu vi tảo trên các sông hồ tại Nghệ An (tỷ lệ 1:6, nguồn ảnh Internet và bản đồ Google)
*Thiết bị, dụng cụ: Cân phân tích (Mettler Toledo, Thụy Sĩ); máy đo độ ẩm tự động (ADAM AMB, Anh); kính hiển vi (Olympus CK90, Nhật bản) có kết hợp máy ảnh; kính hiển vi ngược (Axiovert 40 CFL, Đức); buồng đếm tế bào (Fisher, Hoa Kỳ); máy quang phổ (BioTek, Hoa Kỳ); tủ ấm CO2; tủ lạnh sâu -80oC; bình nitơ lỏng; cân phân tích; máy đo pH, máy siêu âm ((40 MHz, 180W, Jeken PS-30 Ultrasonic cleaner, Emin, Trung Quốc) và các dụng cụ thí nghiệm thông thường.
2.2. Phương pháp nghiên cứu
- Phương pháp thu mẫu
Sử dụng vợt phù du (dạng hình chóp, có đường kính miệng lưới là 30 cm, chiều dài 0,7 m và đường kính mắt lưới từ 4, 10, 30 và 120 µm) (Hình 2) để thu những loại tảo phù du sống trong hệ sinh thái thủy vực. Ngoài ra, các phương pháp khác như li tâm, lọc, màng lọc hay để lắng mẫu cũng được dùng để thu mẫu tảo phù du nước (ao, hồ, sông,…).

Hình 2. Lưới vợt thu tảo phù du
Mẫu định tính: Thu mẫu tại 4-5 vị trí/thuỷ vực, sau đó trộn mẫu đã thu thành 1 mẫu. Thể tích thu khoảng 500 mL/mẫu, và bảo quản bằng formalin 5% ngay tại hiện trường.
Mẫu phân lập: Thực hiện tương tự và bảo quản ở 4oC.
- Phương pháp làm giàu vi tảo
Mẫu tự nhiên (trừ mẫu tảo đang nở hoa) được bổ sung thêm môi trường thích hợp, pha loãng theo tỉ lệ 1/10 (hoặc 1/20) và được ủ ở điều kiện ánh sáng và nhiệt độ thích hợp (từ một vài ngày đến một vài tuần) để gia tăng mật độ của các tế bào tảo.
- Phương pháp phân lập bằng tách tế bào đơn bằng micropipette
Tế bào đơn hay sợi có thể được nhặt ra dưới kính hiển vi phân tích nhờ Pasteur micropipette. Quy trình phân lập được thực hiện như trong tài liệu [9] để thu được đơn tế bào và nuôi cấy đơn bào.
- Phương pháp phân tích mẫu
Sử dụng kính hiển vi (Olympus CK90) có kết hợp máy ảnh để kiểm tra và xác định hình thái của các loài vi tảo trong các mẫu nước. Ảnh chụp được xử lý phân loại bằng phần mềm Adobe Photoshop CS3 Extended Version 10.0. Phân loại dựa vào hệ thống phân loại mới của Hoffmann và cộng sự [10, 11].
- Phương pháp tạo dịch chiết vi tảo
Phương pháp chiết với dung môi methanol (MeOH) có hỗ trợ siêu âm được sử dụng để tạo cặn chiết MeOH từ sinh khối các loài vi tảo. Tóm tắt: Vi tảo sau khi được thu tại nguồn, làm sạch, phân lập và làm giàu được đem lọc qua màng lọc để loại bỏ hết nước. Sinh khối vi tảo dính trên màng lọc được đem phơi khô, cân trọng lượng, nghiền thành bột mịn và đem chiết với dung môi MeOH (tỷ lệ sinh khối vi tảo:MeOH (1:20, v/v)) rồi siêu âm trong 3 giờ ở nhiệt độ 40-50 oC. Sau khi siêu âm, hỗn hợp sinh khối vi tảo được lọc thu lấy dịch chiết. Dịch chiết thu được đem cô quay dưới áp suất giảm ở nhiệt độ 50oC để cất loại dung môi và thu lấy cặn chiết MeOH. Khối lượng cặn chiết MeOH các mẫu vi tảo, được trình bày trong Bảng 1.
- Phương pháp thử nghiệm hoạt tính gây độc tế bào
Phương pháp SRB được sử dụng để đánh giá hoạt tính gây độc tế bào ung thư in vitro của các cặn chiết MeOH từ các loài vi tảo nghiên cứu [12]. Phép thử được thực hiện theo như trong tài liệu [13]. Phép thử được lặp lại 3 lần. Ellipticine được sử dụng là chất đối chứng tham khảo. DMSO 1% được sử dụng như đối chứng âm (nồng độ cuối cùng trong giếng thử là 0,05%). Kết quả OD ở bước sóng 540 nm trên máy ELISA Plate Reader (BioTek, Hoa Kỳ). Số liệu được xử lý trên phần mềm Excel 2019.
3. KẾT QUẢ NGHIÊN CỨU
3.1. Kết quả thu mẫu, định danh, làm giàu và tạo dịch chiết MeOH từ vi tảo
3.1.1. Kết quả thu mẫu tại khu vực Nghệ An
Tại khu vực Nghệ An, chúng tôi đã tiến hành thu mẫu tại 5 thuỷ vực đại diện cho các thuỷ vực như ao, hồ, hồ chứa và sông: Hồ Goong, Sông Lam, Hồ Thủy Điện Bản Vẽ, đầm nuôi tôm Quỳnh Lưu và Hồ Vực Mấu. Tại mỗi thuỷ vực: 4-5 vị trí được lựa chọn thu mẫu vi tảo (Hình 1). Tổng lượng mẫu thu là 25 mẫu.
3.1.2. Kết quả định danh, phân lập và làm giàu mẫu vi tảo tại khu vực Nghệ An
Từ các mẫu nước thu tại khu vực Nghệ An (thời gian thu mẫu 15/11/2024 - 30/11/2024), 19 chủng vi tảo đã được phân lập và định danh thuộc 3 ngành tảo là Tảo lục (Chlorophyta), Tảo silic (Bacillariophyta), và vi khuẩn lam (Cyanopbacteria), bao gồm:
- Ngành Tảo lục (Chlorophyta): Chlorella vulgaris và Scenedesmus acuminatus.
- Ngành Tảo silic (Bacilariophyta): Cyclotella sp. và Amphora sp..
- Vi khuẩn lam: Aphanizomenon sp., Microcystis aeruginosa, Anabaena sp., Anabaena circinalis, Microcystis wesenbergii, Nostoc calcicola, Aphanizomenon flos-aquae, Spirulina platensis, Spirulina maxima, Microcystis sp.XO1, Hapalosiphon welwitschii, Mastigocladus sp., Westiellopsis prolifica, Nostoc sp4. và Nostoc sp5.
Địa điểm thu mẫu trình bày tại bảng 1 và hình ảnh của các mẫu vi tảo định danh được trình bày ở hình 3.
3.1.3. Kết quả tạo dịch chiết MeOH các mẫu vi tảo
Sinh khối của 19 loài vi tảo (3 L /bình) lần lượt được chiết với MeOH thu được các cặn chiết được trình bày trong bảng 1. Kết quả cho thấy hiệu suất thu cặn chiết MeOH từ sinh khối các loài vi tảo nằm trong khoảng 10,0-14,5%.
3.2. Kết quả tác dụng kháng các dòng tế bào ung thư của các cặn chiết vi tảo thu tại Nghệ An
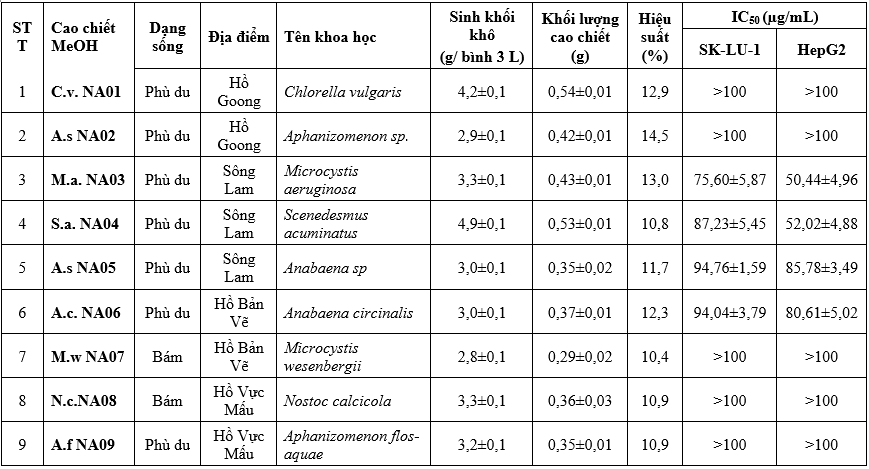
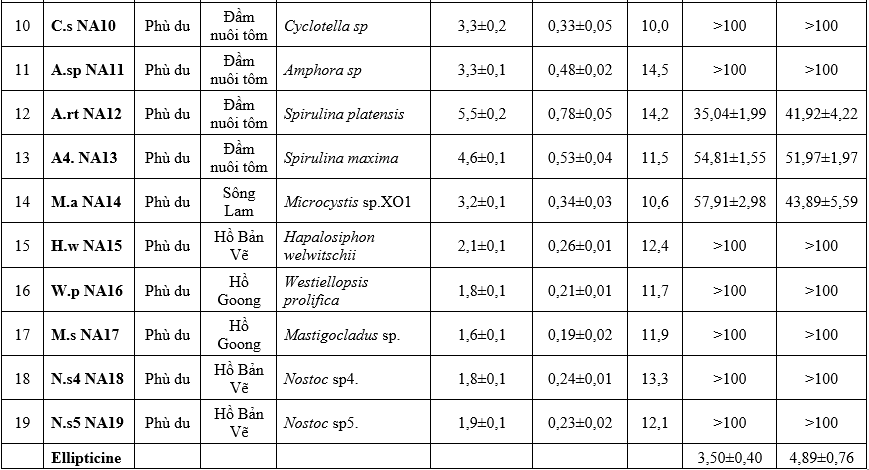
Cặn chiết MeOH của các chủng vi tảo được đánh giá hoạt tính gây độc tế bào ung thư trên các dòng tế bào ung thư phổi SK-LU-1 và ung thư gan HepG2. Kết quả thử nghiệm tác dụng độc tế bào ung thư được trình bày trong bảng 1.
Kết quả nghiên cứu cho thấy 7/19 mẫu nghiên cứu thể hiện khả năng ức chế cả hai dòng tế bào ung thư HepG2 và SK-LU-1 là Microcystis aeruginosa NA03, Scenedesmus acuminatus NA04, Anabaena sp NA05, Anabaena circinalis NA06, Spirulina platensis NA12, Spirulina maxima NA13 và Microcystis sp. NA14 với giá trị IC50 trong khoảng 35,04 - 94,76 μg/mL (SK-LU-1) và 41,92 - 85,78 μg/mL (HepG2) và 12/19 mẫu không thể hiện hoạt tính ở các nồng độ nghiên cứu (IC50 > 100 μg/mL) (Bảng 1).
Đáng chú ý là các mẫu vi tảo Spirulina platensis NA12 và S. maxima NA13 và mẫu Microcystis sp. NA14 thể hiện tác dụng gây độc tế bào ung thư với giá trị IC50 thấp từ 35,04-57,91 μg/mL (SK-LU-1) và 41,92- 51,97 μg/mL (HepG2).
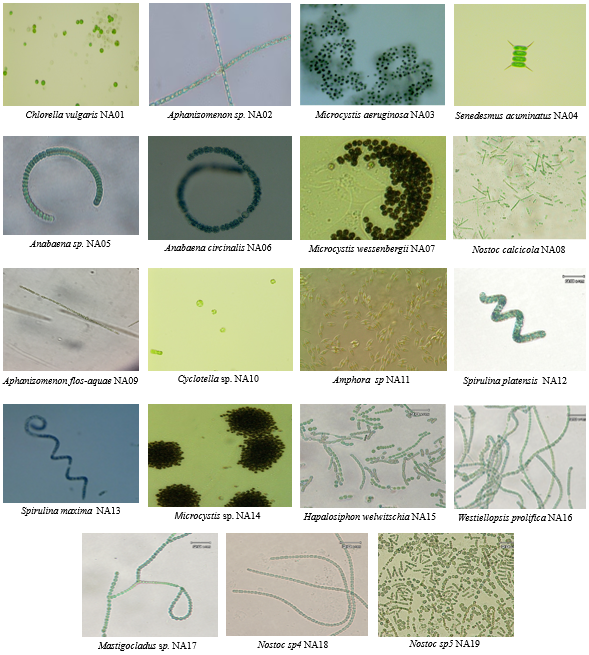
Hình 3. Hình ảnh các mẫu vi tảo thu tại Nghệ An
Bảng 1. Thông tin về mẫu và hoạt tính gây độc tế bào ung thư của các mẫu vi tảo thu tại Nghệ An
4. BÀN LUẬN
Từ các mẫu nước thu mẫu ở tại 5 thuỷ vực ở khu vực Nghệ An bao gồm: Hồ Goong, Sông Lam, Hồ Thủy Điện Bản Vẽ, đầm nuôi tôm Quỳnh Lưu và Hồ Vực Mấu với tổng số có 25 điểm thu mẫu (thời gian thu mẫu từ ngày 15/11/2024 đến ngày 30/11/2024), chúng tôi đã phân lập được 19 chủng vi tảo và vi khuẩn lam thuộc ba ngành tảo lục, tảo silic và vi khuẩn lam với tên định danh khoa học được liệt kê trong bảng 1.
Các mẫu vi tảo sau khi được thu tại các hồ và sông tại khu vực Nghệ An, được làm giàu để tạo thành các sinh khối tảo nuôi trồng trong môi trường nhân tạo. Các vi tảo này sau đó được đem lọc, sấy khô, và chiết lấy dịch MeOH có hỗ trợ siêu âm. Dịch chiết MeOH được lọc bỏ bã, đem cô quay dưới áp suất giảm để thu được cặn chiết MeOH vi tảo tương ứng. Khối lượng của các cặn chiết MeOH vi tảo thu được ở Nghệ An (19 mẫu) được trình bày ở bảng 1. Hiệu suất thu cặn chiết MeOH từ sinh khối các loài vi tảo nằm trong khoảng 10,00-15,33%.
Kết quả thử nghiệm tác dụng độc tế bào cho thấy, trong số 19 mẫu cặn chiết vi tảo thu tại Nghệ An thì có 7 mẫu có hoạt tính bao gồm 2 mẫu Microcystic (M. aeruginosa NA03) và (Microcystis sp. NA14), 2 mẫu Anabaena (Anabaena sp. NA05)và (A. circinalis NA06)), 2 mẫu Spirulina là (S. platensis NA12) và (S. maxima NA13)) và một mẫu Senedemus (S. acuminatus NA04) với giá trị IC50 trong khoảng 35,04±1,99 - 94,76±1,59 (μg/mL) (kháng SK-LU-1) và 41,92±4,22 - 85,78±3,49 (μg/mL) (kháng HepG2). Trong đó, 02 mẫu vi tảo S. platensis NA12, S. maxima NA13và mẫu Microcystis sp. NA14 có giá trị IC50 thấp, lần lượt là 35,04±1,99, 54,81±1,55 và 57,91±2,98 (μg/mL) (SK-LU-1) và 41,92±4,22, 51,97±1,97 và 43,89±5,59 (μg/mL) (HepG2) (Hình 2).
2 mẫu Spirulina là (S. platensis NA12) và S. maxima NA13) đều là những mẫu tảo xoắn thu tại ao nuôi tôm tại Nghệ An, một loại vi khuẩn lam dạng sợi xoắn màu xanh lục. Độc tính của vi tảo này có thể gây ra là do hàm lượng kim loại nặng như Cd, Pb or Hg tích lũy trong tảo trong môi trường nước tù đọng nhiều. Tảo xoắn có tác dụng bảo vệ tế bào (như tế bào thần kinh) khỏi độc tính của kim loại nặng [15]. Spirulina platensis với các thành phần phenolic hữu cơ như quercetin (214,06 ppm), kaempferol (126,45 ppm), resorcinol (27,02 ppm) và naphthaline (2,42 ppm) (phân tích bằng HPLC) cũng là chất trừ sâu tự nhiên chống lại trùng hại lá bông Spodoptera littoralis [16].
Microcystis sp. NA14 là mẫu vi tảo thu tại sông Lam, Nghệ An thể hiện tác dụng độc tế bào ung thư khá mạnh trên cả 2 dòng tế bào ung thư. Microcystic sp. là những vi khuẩn lam sinh độc tố tiêu biểu trong nước ngọt. Peptide microcystin tiết ra trong môi trường nước trong các đợt tảo xanh Microcystis và Anabaena nở hoa được coi là chất độc tảo lam (cyanotoxin) gây độc cho người và các loài động vật thủy sinh [17,18].
5. KẾT LUẬN
Chúng tôi đã tiến hành thực hiện nghiên cứu, phân lập và định danh được 19 mẫu vi tảo tại các điểm khác nhau thuộc các sông và hồ nước ngọt thuộc tỉnh Nghệ An. Sau khi phân lập, làm giàu và tạo cặn chiết MeOH, các cặn chiết MeOH vi tảo được đánh giá hoạt tính gây độc tế bào trên 02 dòng tế bào ung thư phổi SK-LU-1 và ung thư gan HepG2. Trong đó 7 mẫu thể hiện khả năng ức chế cả hai dòng tế bào ung thư HepG2 và SK-LU-1 với giá trị IC50 trong khoảng 35,04-94,76 μg/mL (SK-LU-1) và 41,92-85,78 μg/mL (HepG2). Các mẫu S. platensis NA12 và S. maxima NA13 và Microcystis sp. NA14 có giá trị IC50 thấp, từ 35,04-57,91 μg/mL (SK-LU-1) và 41,92-51,97 μg/mL (HepG2). Tác dụng gây độc tế bào ung thư mạnh của chúng có thể là do các hoạt chất sinh học, thường là các chất độc cho người và động vật như cyanotoxin chúng tiết ra trong quá trình phát triển (hiện tượng tảo nở hoa). Kết quả nghiên cứu đã bổ sung vào danh mục các chủng vi tảo tiềm năng làm tiền đề cho nghiên cứu các hoạt chất sinh học từ vi tảo. Trong tương lai, cần có các nghiên cứu sâu thêm về thành phần hóa học của các loài vi tảo này để phát hiện ra các chất có hoạt tính sinh học, đặc biệt là tác dụng chống ung thư để nghiên cứu sử dụng làm thuốc.
Lời cảm ơn: Nghiên cứu này được tài trợ kinh phí bởi Bộ Khoa học và Công nghệ (Mã số đề tài: ĐTĐLCN-76/22).
Tuyên bố về sử dụng Gen AI: Các tác giả khẳng định rằng không sử dụng bất kỳ công cụ AI tạo sinh nào để tạo hoặc chỉnh sửa nội dung khoa học của bản thảo này. Mọi phân tích, diễn giải và kết luận hoàn toàn do các tác giả thực hiện.
Tuyên bố về đóng góp của tác giả: Phạm Ngọc Khanh: Viết draft bài báo; Nguyễn Thị Minh Hằng: Khái niệm hóa, phương pháp luận; Dương Thị Thủy, Nguyễn Thị Thu Liên, Trần Hữu Giáp: Thu vi tảo; Dương Thị Thủy, Nguyễn Thị Thu Liên: Phân lập vi tảo; Nguyễn Trọng Dân, Nguyễn Tú Oanh: Làm giàu, tạo cao chiết MeOH vi tảo; Đỗ Thị Thảo, Nguyễn Thị Thu Hà: Thử nghiệm tác dụng sinh học; Nguyễn Xuân Nhiệm: Phụ trách triển khai đề tài.
Tuyên bố về xung đột lợi ích: Các tác giả tuyên bố không có xung đột lợi ích liên quan đến nghiên cứu này.
Tài liệu tham khảo
- L. Barsanti et al., Oddities andcuriosities in the algal world in Algal Toxins: Nature, occurrence, effect and detection. Dordrecht, Springer Netherlands, 2008.
- L. Barsanti, P. Gualtieri, Algae: Anatomy, biochemistry and biotechnology. CRC Press., 2014, 361 p.
- I. Priyadarshani, B. Rath, Bioactive compounds from microalgae and cyanobacteria: utility and applications, International Journal of Pharmaceutical Sciences and Research, Vol. 3, No.11, pp. 4123-4130, 2012. DOI: 10.13040/IJPSR.0975-8232.3(11)
- M. Schumacher, J. Yanık, A. Sınağ and A. Kruse, Hydrothermal conversion of seaweeds in a batch autoclave, The Journal of Supercritical Fluids, Vol. 58, pp. 131-135, 2011. DOI: 10.1016/j.supflu.2011.04.009
- Y.V. Yuan, N.A. Walsh, Antioxidant and antiproliferative activities of extracts from a variety of edible seaweeds, Food and Chemical Toxicology, Vol. 44, pp. 1144-1150, 2006. DOI: 10.1016/j.fct.2006.02.002
- X. Liu, A.F. Clarens and L.M. Colosi, Algae biodiesel has potential despite inconclusive results to date, Bioresource Technology, Vol. 104, pp. 803-806, 2012. DOI: 10.1016/j.biortech.2011.10.077
- M.G. de Morais, S. Vaz Bda, E.G. de Morais and J.A. Costa, Biologically active metabolites synthesized by microalgae, Biomed Research International, Vol. 2015, pp. 835761, 2015. DOI: 10.1155/2015/835761
- A.M. Burja, B. Banaigs, E. Abou-Mansour, J.G. Burgess and P.C. Wright, Marine cyanobacteria - a prolific source of natural products, Tetrahedron, Vol. 57, pp. 9347-77, 2001. DOI: 10.1016/S0040-4020(01)00931-0
- S. Fernandez-Valenzuela, F. Chávez-Ruvalcaba, J.C. Beltran-Rocha, P.M. San Claudio and R. Reyna-Martínez, Isolation and culturing axenic microalgae: Mini–review, The Open Microbiology Journal, Vol. 15, pp. 111-119, 2021. DOI: 10.2174/1874285802115010111
- L. Hoffmann, Nomenclature of Cyanophyta/Cyanobacteria: roundtable on the unification of the nomenclature under the botanical and bacteriological codes, Algological Studies, Vol. 117, pp. 13-29, 2005. DOI: 10.1127/1864-1318/2005/0117-0013
- P. Rajaniemi et al., Phylogenetic and morphological evaluation of the genera Anabaena, Aphanizomenon, Trichormus and Nostoc (Nostocales, Cyanobacteria), International Journal of Systematic and Evolutionary Microbiology, Vol. 55, No. 1, pp. 11-26, 2005. DOI: 10.1099/ijs.0.63276-0
- P. Skehan et al., New colorimetric cytotoxicity assay for anticancer-drug screening, Journal of the National Cancer Institute, Vol. 82, No. 13, pp. 1107-1112, 1990. DOI: 10.1093/jnci/82.13.1107
- N.V. Thang et al., Oleanane-type saponins from glochidion hirsutum and their cytotoxic activities, Chem Biodivers, Vol. 14, No. 5, pp. e1600445 (1-9), 2017. DOI: 10.1002/cbdv.201600445
- J.P. Hughes, S. Rees, S.B. Kalindjian and K.L. Philpott, Principles of early drug discovery, British Journal of Pharmacology, Vol. 162, No. 6, pp. 1239-1249, 2011. DOI: 10.1111/j.1476-5381.2010.01127.x
- R. Mallamaci, M. Storelli, A. Barbarossa, G. Messina, A. Valenzano and D. Meleleo, Potential protective effects of Spirulina (Spirulina platensis) against in vitro toxicity induced by heavy metals (Cadmium, mercury, and lead) on SH-SY5Y neuroblastoma Cells, International Journal of Molecular Sciences, Vol. 24, No. 23, pp. 17076, 2023. DOI: 10.3390/ijms242317076
- R.S. Rashwan, D.M. Hammad, Toxic effect of Spirulina platensis and Sargassum vulgar as natural pesticides on survival and biological characteristics of cotton leaf worm Spodoptera littoralis, Scientific African, Vol. 8, pp. e00323, 2020. DOI: 10.1016/j.sciaf.2020.e00323
- K. Kameyama, N. Sugiura, Y. Inamori and T. Maekawa, Characteristics of microcystin production in the cell cycle of Microcystis viridis, Environmental Toxicology, Vol. 19, No. 1, pp. 20-5, 2004. DOI: 10.1002/tox.10147
- R. Melaram, A.R. Newton, and J. Chafin, Microcystin contamination and toxicity: Implications for agriculture and public health, Toxins (Basel), Vo. 14, No. No. 5, pp. 350 (1-18), 2022. DOI: 10.3390/toxins14050350