Nghiên cứu xác định kháng sinh meropenem trong mẫu huyết tương bằng phương pháp huỳnh quang sử dụng tổ hợp CQDs/AuNPs
Khoa Hóa học, Trường Đại học Khoa học Tự nhiên, Đại học Quốc gia Hà Nội
19 Lê Thánh Tông, Hoàn Kiếm, Hà Nội
Số điện thoại: 0982384588; Email: m.t.n.pham@gmail.com
Nội dung chính của bài viết
Tóm tắt
Nghiên cứu hướng tới phát triển qui trình xác định nồng độ kháng sinh meropenem dựa trên tín hiệu độ phục hồi huỳnh quang của hệ vật liệu nano bao gồm chấm lượng tử carbon và hạt nano vàng (CQDs/AuNPs). Dung dịch CQDs có khả năng phát huỳnh quang rất mạnh, nhưng cường độ huỳnh quang của dung dịch giảm mạnh khi có mặt AuNPs do xảy ra hiện tượng truyền năng lượng cộng hưởng giữa AuNPs và CQDs. Khi meropenem được thêm vào hệ CQDs/AuNPs, meropenem tương tác mạnh với các hạt nano vàng (AuNPs) và tách CQDs ra khỏi bề mặt AuNPs, từ đó phục hồi tín hiệu huỳnh quang của hệ. Tại các điều kiện tối ưu (pH 2, CuSO4 0,1 mM), hệ CQDs/AuNPs cho thấy khả năng hiệu quả trong việc định lượng meropenem ở mức nồng độ rất thấp (ppb) chỉ sau 8 phút ủ. Kết quả đã chứng minh mối tương quan tuyến tính giữa tín hiệu huỳnh quang phục hồi và nồng độ meropenem trong khoảng từ 2×10⁻⁸ M đến 5×10⁻⁶ M. Phương pháp đã được áp dụng thành công để định lượng hàm lượng meropenem trong mẫu huyết tương người.
Abstract
Fluorescence detection of antibiotic meropenem in human plasma using CQDs/AuNPs
In this study, meropenem is detected by fluorescence recovery signals of carbon quantum dots and nanoparticles (CQDs/AuNPs) nanocomposite. CQDs strongly fluoresce under UV light, but in the presence of AuNPs the fluorescence signal decreases due to the energry transfer between AuNPs and CQDs. Upon the addition of meropenem to the CQDs/AuNPs system, the strong interaction between N-H groups in meropenem molecules and AuNPs leads to the release of CQDs from AuNPs, thereby restores their fluorescence. The CQDs/ AuNPs system can sensitively detect meropenem in aqueous solutions (pH 2.0, CuSO4 0.1 mM) at ppb levels, with a rapid response time of just 8 minutes. Additionally, the recovery of fluorescence exhibits a good linear correlation with the concentration of meropenem in the range of 2.10-8 M to 5.10-6 M. Successful application of the developed method was achieved for determining meropenem in human plasma samples.
Từ khóa
Xác định meropenem, chấm lượng tử carbon, hạt nano vàng, phổ huỳnh quang, Meropenem determination, carbon quantum dots, gold nanoparticle, fluorescence spectrometry
Chi tiết bài viết

Bài báo này được cấp phép theo Creative Commons Attribution 4.0 International License.
- Điểm nổi bật:
Phát triển phương pháp huỳnh quang sử dụng vật liệu CQDs/AuNPs để phát hiện và định lượng meropenem.
Cơ chế phát hiện dựa trên sự phục hồi huỳnh quang khi meropenem tương tác với AuNPs, giải phóng CQDs.
Độ hồi phục huỳnh quang có quan hệ tuyến tính với nồng độ meropenem trong khoảng 2×10⁻⁸ M đến 5×10⁻⁶ M.
Ứng dụng thành công để xác định hàm lượng meropenem trong mẫu huyết tương người.
1. ĐẶT VẤN ĐỀ
Meropenem là một kháng sinh thuộc nhóm carbapenem của β- Lactam (Hình 1), thường được sử dụng trong y học như giải pháp cuối cùng để điều trị các bệnh do nhiễm khuẩn nghiêm trọng, đặc biệt là trong trường hợp bệnh nhân kháng các loại kháng sinh khác do cơ chế ngăn chặn quá trình tổng hợp các loại vi khuẩn của meropenem. Nhờ vào cấu trúc ổn định, kháng sinh này được đánh giá là có tính an toàn cao và mang lại hiệu quả điều trị tốt [1, 2].
Hiện nay, việc sử dụng kháng sinh meropenem rất phổ biến dẫn tới nhu cầu cấp thiết để định tính và định lượng meropenem trong dịch sinh học, góp phần đánh giá dược động học và dược lực học của thuốc đối với bệnh nhân. Tuy nhiên, một số phương pháp phân tích tiêu chuẩn như phương pháp điện hóa [3], phương pháp điện di mao quản [4], phương pháp sắc ký lỏng hiệu năng cao HPLC [5, 6] , v.v. còn tồn tại một số nhược điểm như tốn kém chi phí cho phí vận hành, dung môi hóa chất, nhân lực đào tạo kỹ thuật. Do đó, việc nghiên cứu các cách tiếp cận mới nhằm giảm giá thành và thời gian phân tích nhưng vẫn duy trì hiệu quả chính xác luôn là chủ đề được quan tâm.
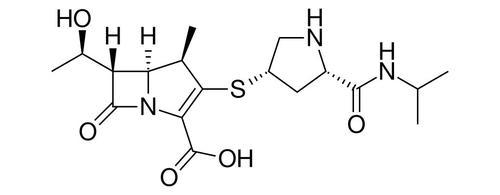
Hình 1. Cấu trúc phân tử của meropenem
Chấm lượng tử carbon (CQDs) với khả năng phát huỳnh quang mạnh được xem là một đại diện tiêu biểu cho hệ vật liệu nano mới nổi có nhiều ứng dụng rộng rãi trong các lĩnh vực. CQDs dễ dàng tổng hợp từ các nguồn tài nguyên sinh khối dồi dào, không bị chuyển hóa thành các chất gây ô nhiễm môi trường. Nhiều nghiên cứu đã sử dụng CQDs để thực hiện phân tích lượng vết các chất dựa trên hiện tượng tăng hoặc giảm huỳnh quang của CQDs khi tiếp xúc với các ion kim loại hoặc hợp chất hữu cơ [7, 8].
Một số công trình trước đây của nhóm nghiên cứu chúng tôi đã sử dụng tổ hợp vật liệu CQDs với hạt nano vàng (CQDs/AuNPs) để phân tích các hợp chất như tyramin trong phomai, amikacin trong dược phẩm [9, 10], .v.v. Nguyên tắc của phương pháp dựa trên tương tác ái lực của nhóm -NH và -SH trong phân tử các chất với hạt nano vàng, từ đó làm suy yếu tương tác giữa hạt nano vàng và CQDs và dẫn đến hiện tượng hồi phục huỳnh quang của hệ CQDs/AuNPs. Trong nghiên cứu này, dựa trên đặc điểm phân tử meropenem cũng chứa các nhóm chức -NH và R–S–R′ có ái lực tốt với các hạt AuNPs, chúng tôi sẽ sử dụng hệ vật liệu CQDs/AuNPs để xác định kháng sinh meropenem với nguyên tắc tương tự. Nhằm tối ưu hóa điều kiện phân tích, các thông số sẽ được khảo sát bao gồm thời gian ủ mẫu, nồng độ muối điện ly, pH. Sau khi đánh giá khả năng sử dụng của phương pháp, phương pháp phân tích sẽ được tiến hành trên mẫu thật là mẫu huyết tương của bệnh nhân đã sử dụng meropenem, đồng thời kết quả phân tích sẽ được so sánh đối chứng với phương pháp LC-MS/MS.
2. VẬT LIỆU VÀ PHƯƠNG PHÁP THỰC NGHIỆM
2.1. Thiết bị và hóa chất
Các hóa chất được sử dụng đều là hóa chất tinh khiết cho phân tích bao gồm: gold (III) chloride trihydrate (HAuCl4.3H2O, 99,9%), meropenem trihydrate (C17H25N3O5S.3H2O, 98%) từ hãng Sigma Aldrich (Mỹ), copper (II) sulfate pentahydrate (CuSO4.5H2O, 99% ), sodium hydroxide (NaOH, 98%), hydrochloric acid (HCl, 37%), citric acid monohydrate(C6H8O7.H2O, 99,5%), sodium citrate dihydrate (Na3C6H5O7.2H2O) từ hãng Xilong (Trung Quốc), chloroform (CHCl3, 99%) của hãng Merck (Đức) và nước deion.
Máy huỳnh quang (F-4700, HITACHI, Nhật Bản) với cuvet tiêu chuẩn chiều dày 1 cm và 4 mặt trong suốt được sử dụng cho phép đo huỳnh quang.
2.2. Tổng hợp CQDs, CQDs/AuNPs từ citric acid
CQDs, CQDs/AuNPs được tổng hợp theo qui trình đã báo cáo trong 1 nghiên cứu trước đây của chúng tôi [9]. CQDs được tổng hợp bằng cách nung 10 g acid citric ở 180oC trong 24 giờ và để nguội tự nhiên ở điều kiện thường. Hòa tan hỗn hợp thu được vào nước deion, loại bỏ phần chất rắn không hòa tan. Phần còn lại được bảo quản trong tủ lạnh 4oC.
Để tổng hợp CQDs/AuNPs, dung dịch CQDs với nồng độ 0,02 mg/mL thu được từ phần trên được trộn với dung dịch HAuCl₄ 1 mM theo tỷ lệ thể tích 1:1 và ủ ở nhiệt độ phòng 30 phút đến khi dung dịch chuyển sang màu đỏ rượu vang. Trong qui trình này, CQDs vừa là tác nhân khử vừa là tác nhân ổn định AuNPs, giúp bảo vệ các hạt AuNPs không bị keo tụ.
2.3. Nguyên tắc xác định meropenem
Dung dịch CQDs lần lượt được kích thích và phát quang tại các bước sóng tương ứng là 360 nm và 445 nm. Khi có mặt AuNPs, cường độ huỳnh quang của dung dịch giảm do hiện tượng truyền năng lượng cộng hưởng giữa CQDs và AuNPs (tương ứng trạng thái tắt). Khi thêm chất phân tích là meropenem, nhóm -NH và -SH của meropenem có ái lực mạnh với Au nên được hấp phụ tốt trên bề mặt Au, cạnh tranh tương tác với CQDs, kìm hãm sự truyền năng lượng cộng hưởng giữa AuNPs và CQDs, giúp tín hiệu phát quang của dung dịch tăng trở lại (trạng thái bật). Nhờ đó, có thể xác định meropenem thông qua hiện tượng “tắt-bật” huỳnh quang. Cơ chế xác định Meropenem được thể hiện trên hình 2.
Để định lượng meropenem, thiết lập mối tương quan giữa độ hồi phục huỳnh quang (F-F0)/F0 tại bước sóng 445 nm và nồng độ meropenem, trong đó F0 và F lần lượt là cường độ huỳnh quang của dung dịch CQDs/AuNPs trước và sau khi thêm meropenem.
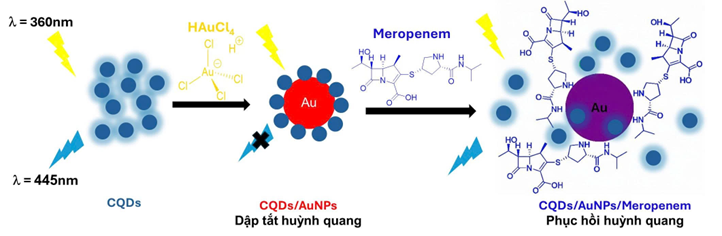
Hình 2. Cơ chế xác định Meropenem dựa trên sự phục hồi huỳnh quang của CQDs
2.4. Xử lý mẫu
Mẫu huyết tương chứa meropenem và không chứa meropenem (mẫu trắng) được thu thập từ khoa Hồi sức tích cực của Bệnh viện Bạch Mai. Bệnh nhân được truyền meropenem với liều lượng 1000 mg/lần, ngày truyền từ 1-3 lần. Meropenem được pha với 100 mL NaCl 0,9% và truyền tĩnh mạch với tốc độ 33 mL/giờ. Mẫu huyết tương được lấy tại các thời điểm: ngay sau khi truyền xong (t = 0 giờ), sau khi truyền xong 2 giờ (t = 2 giờ) và sau khi truyền xong 5 giờ (t = 5 giờ). Mẫu được bảo quản đông lạnh và định lượng trong vòng 7 ngày sau khi lấy.
Qui trình chuẩn bị mẫu huyết tương được thực hiện tương tự một nghiên cứu trước đây của chúng tôi khi sử dụng phổ hấp thụ phân tử UV-Vis để xác định nồng độ meropenem [10]: Trộn đều 1 mL mẫu huyết tương với 1 mL acetonitril rồi ly tâm. Chỉnh pH dung dịch sau khi ly tâm đến pH= 5 bằng HCl 0,1 M. Chiết dung dịch thu được bằng 3 mL dung dịch chloroform, lắc trong vòng 15 phút. Ly tâm để tách lớp, thu lấy dung dịch chloroform phía dưới. Cô nitơ dung dịch này đến khô rồi hòa tan vào 2 mL nước cất.
Thêm 20 µL dung dịch CuSO4 0,01M vào 1 mL dung dịch CQDs/AuNPs, điều chỉnh pH dung dịch đến 2. Thêm 200 µL mẫu dung dịch cần phân tích và định mức dung dịch đến 2 mL bằng nước cất. Sau 8 phút, đo cường độ huỳnh quang của dung dịch ở bước sóng 445 nm. Sử dụng phương pháp thêm chuẩn để tính toán hàm lượng meropenem trong mẫu.
3. KẾT QUẢ
3.1. Nghiên cứu ảnh hưởng của các điều kiện phân tích
Để tối ưu qui trình phân tích meropenem sử dụng hệ N-CQDs/AuNPs, chúng tôi tiến hành khảo sát các yếu tố ảnh hưởng đến độ hồi phục huỳnh quang ((F-F0)/F0) của dung dịch, bao gồm: dung dịch muối điện ly, pH dung dịch, thời gian ủ (thời gian meropenem tương tác với AuNPs), ...
3.1.1. Ảnh hưởng của muối điện ly
Sự có mặt của muối điện ly làm giảm lớp điện kép trên bề mặt AuNPs, tăng cường liên kết tĩnh điện giữa AuNPs và meropenem và dẫn đến tăng cường hiệu ứng hồi phục huỳnh quang. Kết quả khảo sát với 6 loại muối điện ly khác nhau bao gồm KNO3, KCl, NaCl, CuSO4, Na2SO4 và K2SO4 cho thấy độ hồi phục huỳnh quang đạt giá trị cao nhất khi sử dụng CuSO4 0,1 mM (Hình 3).
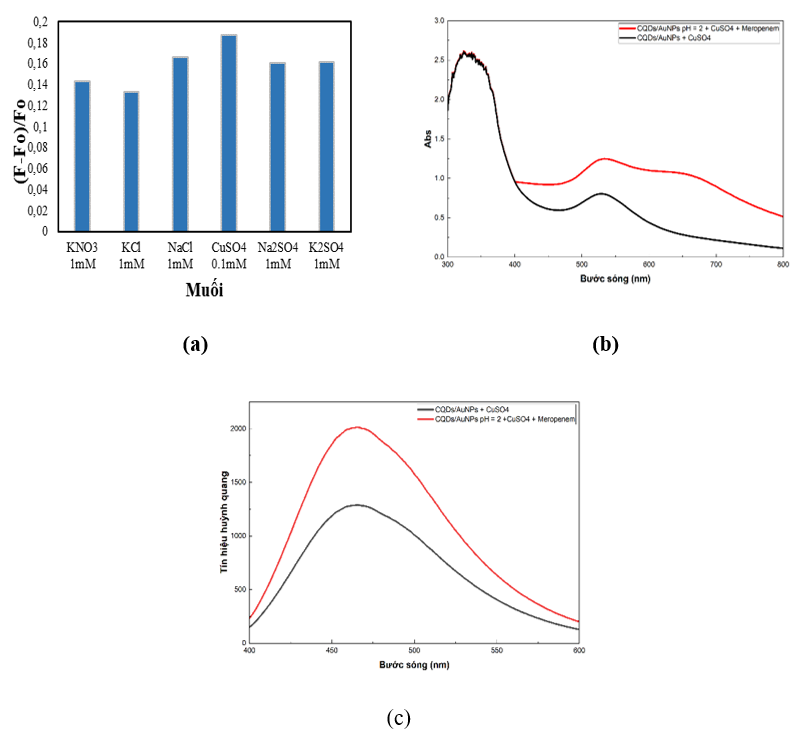
Hình 3. (a) Ảnh hưởng của muối điện ly đến độ hồi phục huỳnh, (b) Phổ hấp thụ của CQDs/AuNPs ở pH = 2 với CuSO4 và Meropenem, (c) Phổ phát xạ của CQDs/AuNPs ở pH = 2 với CuSO4 và Meropenem
3.1.2. Ảnh hưởng của pH
Giá trị pH của dung dịch đóng vai trò quan trọng trong định lượng meropenem, do pH quyết định điện tích của meropenem và liên quan trực tiếp đến tương tác tĩnh điện giữa meropenem và nano vàng [11]. Khi khảo sát độ hồi phục huỳnh quang với pH thay đổi từ 2 ÷ 9, kết quả cho thấy tại pH = 2, độ hồi phục huỳnh quang đạt mức cao nhất khi có mặt meropenem (Hình 4). Do vậy, các thí nghiệm sau đó được thực hiện ở pH = 2.
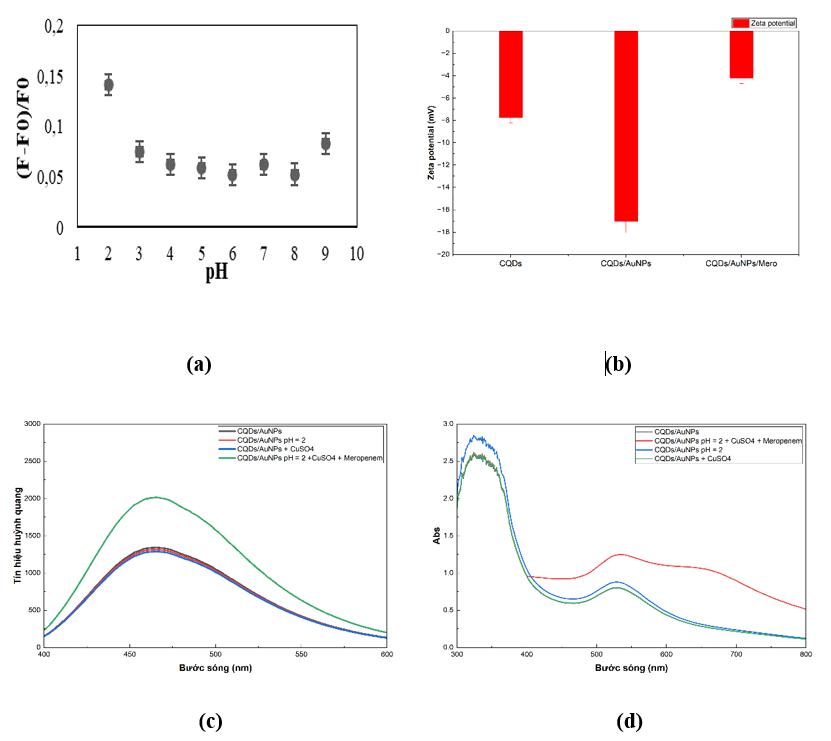
Hình 4. (a) Sự thay đổi pH ảnh hưởng tới độ hồi phục huỳnh quang, (b) Thế zeta của CQDs, CQDs/AuNPs, CQDs/AuNPs/Meropenem, (c) Phổ huỳnh quang của CQDs/AuNPs tại các điều kiện tối ưu, (d) Phổ hấp thụ của CQDs/AuNPs tại các điều kiện tối ưu
3.1.3. Ảnh hưởng của thời gian ủ
Thời gian ủ quyết định mức độ tương tác giữa meropenem và các hạt AuNPs từ đó giải phóng N-CQDs tự do. Khi tiến hành đánh giá ảnh hưởng của thời gian ủ trong vòng 15 phút, kết quả chỉ ra rằng tín hiệu huỳnh quang (ở 445 nm) tăng lên nhanh chóng cho đến phút thứ 8 (Hình 5). Điều này chứng tỏ rằng meropenem đã lập tức phản ứng với AuNPs và sau 8 phút đã bắt đầu bão hòa.
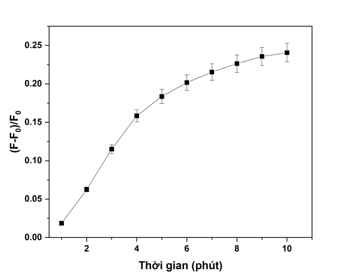
Hình 5. Ảnh hưởng thời gian ủ chất phân tích tới độ hồi phục huỳnh quang
3.1.4. Ảnh hưởng của nồng độ meropenem
Để định lượng meropenem cần tìm được mối quan hệ giữa độ hồi phục huỳnh quang và nồng độ meropenem. Kết quả biểu diễn độ hồi phục huỳnh quang thay đổi theo nồng độ của meropenem từ 1 đến 2x104 nM tại các điều kiện được lựa chọn: pH = 2, thời gian ủ: 8 phút, nồng độ muối CuSO4 0,1 mM được cho trên hình 5. Từ hình 6 cho thấy, tăng nồng độ meropenem dẫn tới tăng tuyến tính tín hiệu hồi phục huỳnh quang (ở 445 nm) trong khoảng nồng độ từ 20 nM đến 5000 nM.
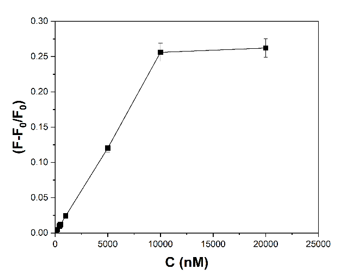
Hình 6. Ảnh hưởng của nồng độ meropenem đến độ hồi phục huỳnh quang
3.2. Đánh giá phương pháp
3.2.1. Xây dựng đường chuẩn, độ chụm, độ đúng, LOD, LOQ
Dựa trên số liệu độ hồi phục huỳnh quang tại các nồng độ meropenem trong khoảng nồng độ từ 20 đến 5000 nM, thiết lập phương trình đường chuẩn: y = 0,2408x + 0,0933, trong đó y là độ hồi phục huỳnh quang (F-F0)/F0, x là nồng độ meropenem tính theo nM. Hệ số tương quan thu được của đường chuẩn là R2= 0,9986.
Các phép đo được thực hiện lặp lại 5 lần để đánh giá độ chụm và độ đúng ở các mức nồng độ 50 nM, 500 nM và 5000 nM. Độ lệch chuẩn tương đối (% RSD) là 4,588%, 4,260% và 2,462% tương ứng với 3 nồng độ, hiệu suất thu hồi của phương pháp dao động từ 95,1% - 109,3%.
Giá trị LOD và LOQ được tính theo công thức LOD =3Sb/b và LOQ = 10Sb/b, trong đó Sb là độ lệch chuẩn của mẫu trắng và b là hệ số góc của đường chuẩn có giá trị tương ứng là 5 nM (2 ppb) và 15 nM (6 ppb).
Bảng 1. Bảng giá trị Sb, Slope b, LOD, LOQ

3.2.2. Độ chọn lọc của phương pháp
Để khảo sát ảnh hưởng của các kháng sinh đối với việc xác định meropenem, chúng tôi đã tiến hành thí nghiệm với các kháng sinh thuộc họ beta lactam bao gồm ertapenem, penicilin V, cefalexin, amocixilin với nồng độ là 10-7 M và các kháng sinh thuộc các họ khác như ciprofloxacin, amikacin, tetracyclin (Hình 7). Kết quả cho thấy trừ ertapenem là kháng sinh cùng nhóm carbapenem với meropenem, các kháng sinh khác đều cho đáp ứng hồi phục huỳnh quang không đáng kể với dung dịch CQDs/AuNPs.
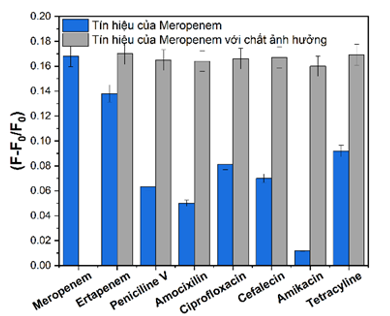
3.3. Kết quả xác định meropenem trong các mẫu thực
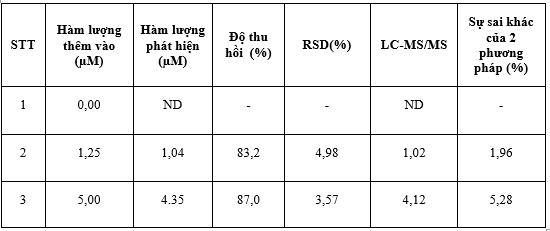
Kết quả xác định độ thu hồi trên nền mẫu huyết tương trắng cho thấy khi thêm chuẩn meropenem ở các nồng độ 1,25 và 5,00 µM, hiệu suất thu hồi (H%) tương đối tốt, đạt từ 83,2 đến 87,1%, với độ lệch chuẩn tương đối (RSD%) từ 5,6 đến 8,9% (n=3), (Bảng 2) tuân thủ các tiêu chí của AOAC áp dụng cho phân tích.
Bảng 2. Kết quả đo mẫu huyết tương trắng bằng phương pháp thêm chuẩn
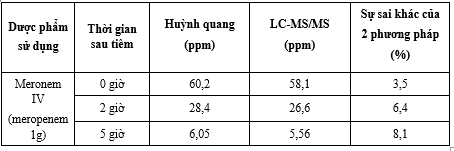
Kết quả phân tích mẫu huyết tương của bệnh nhân được tiêm truyền meropenem, được cho trong bảng 3. Nồng độ meropenem trong huyết tương sau khi tiêm là 60,2 ppm, sau 2 h tiêm là 28,4 ppm và sau 5 h tiêm nồng độ còn lại trong huyết tương chỉ duy trì ở 6,05 ppm.
Bảng 3. Hàm lượng mẫu huyết tương được xác định bằng phương pháp huỳnh quang và LC-MS/MS
4. THẢO LUẬN
4.1. Ảnh hưởng của các điều kiện phân tích
Kết quả tối ưu các điều kiện phân tích meropenem khi có mặt hệ vật liệu CQDs/Au cho thấy độ hồi phục huỳnh quang đạt cực đại tại các điều kiện pH = 2, thời gian ủ: 8 phút, nồng độ muối CuSO4 0,1 mM. Có thể thấy các điều kiện tối ưu tương ứng với độ hồi phục huỳnh quang cực đại đạt được khi tương tác giữa chất phân tích là meropenem và AuNPs là lớn nhất. Độ hồi phục huỳnh quang đạt cực đại ở pH 2 có thể được giải thích là do ở pH < pKa = 2.9, nhóm NH2+ của meropenem mang điện tích dương, còn các hạt nano vàng được bảo vệ bởi lớp vỏ CQDs tích điện âm (Hình 4b). Tương tác tĩnh điện giữa meropenem và nano Au khi đó rất mạnh. Khi tăng pH, meropenem tích điện âm hơn do nhóm COOH bị phân ly và hơn thế nữa nhóm NH2 lúc này trở nên không mang điện tích do đó meropenem khó bị hấp phụ hơn trên bề mặt tích điện âm của nano Au. Với pH giá trị dưới 2, các hạt AuNPs có xu hướng kết tụ và làm đổi màu dung dịch khi không có chất phân tích.
Kết quả khảo sát ảnh hưởng của muối điện ly cho thấy vai trò quan trọng của các ion đến tương tác của meropenem và AuNPs. Trong số các muối điện ly đã khảo sát bao gồm KNO3, KCl, NaCl, CuSO4, Na2SO4 và K2SO4, muối CuSO4 cho tín hiệu cao nhất có thể do đây là muối của các ion hóa trị 2, cho giá trị lực ion cao nhất và tác động lớn nhất đến việc giảm lớp điện kép xung quanh AuNPs và tăng cường tương tác liên kết tĩnh điện giữa AuNPs và meropenem.
4.2. Đánh giá phương pháp
Tại các điều kiện tối ưu, độ hồi phục huỳnh quang thay đổi theo nồng độ của meropenem trong khoảng nồng độ từ 20 nM đến 5000 nM. Hệ số tương quan thu được của đường chuẩn là R2 = 0,9986, cho thấy mối quan hệ tuyến tính cao giữa độ hồi phục huỳnh quang và nồng độ meropenem, có thể áp dụng để phân tích meropenem trong các đối tượng mẫu có nồng độ thấp.
Khi đánh giá khả năng sử dụng của phương pháp theo tiêu chuẩn của AOAC, các giá trị độ lệch chuẩn tương đối (RSD%) dao động trong khoảng từ 2,46% đến là 4,58% và hệ số thu hồi (H%) dao động trong khoảng từ 95,1% - 109,3% đáp ứng yêu cầu đặt ra của AOAC (H% từ 80 - 110%, RSD < 15% ở mức nồng độ 100 ppb).
Giá trị LOD và LOQ của phương pháp tương ứng là 5 nM (2 ppb) và 15 nM (6 ppb), thấp hơn rõ rệt khi so sánh với các phương pháp như điện di mao quản (2 ppm) [12], UV-Vis (0,19 ppm) [13], HPLC-UV (1,06 ppm) [14]. Giá trị này xấp xỉ với phương pháp LC/MS (0,015 ppm) [15], cho thấy hiệu quả vượt trội của một phương pháp quang học đơn giản trong việc xác định lượng vết của kháng sinh.
Ngoài ra, phương pháp cũng thể hiện độ chọn lọc tốt, không bị ảnh hưởng bởi các kháng sinh thuộc họ beta lactam như penicilin V, cefalexin, amocixilin và các kháng sinh thuộc các họ khác như ciprofloxacin, amikacin, tetracyclin. Các kháng sinh thuộc họ beta lactam mặc dù cũng chứa các nhóm chức có liên kết ái lực với AuNPs như thiolether, amine nhưng cấu trúc không gian đã cản trở các nhóm chức này liên kết với AuNPs. Các kháng sinh còn lại chỉ có nhóm chức amine là có khả năng tương tác tốt với các hạt AuNPs, nhưng tương tác này chưa đủ thắng được lực tương tác giữa CQDs và AuNP và phá vỡ liên kết giữa CQDs và AuNPs. Ertapenem là kháng sinh cùng nhóm carbapenem với meropenem có đáp ứng tương tự, có thể gây ảnh hưởng đến kết quả và đây là một trong các hạn chế của phương pháp. Tuy nhiên việc sử dụng đồng thời các kháng sinh trong cùng 1 nhóm để điều trị bệnh nhân là không phổ biến. Đánh giá chung cho thấy phương pháp có độ đúng, độ chụm và độ chọn lọc tốt, phù hợp để phân tích meropenem trong nền mẫu phức tạp như mẫu huyết tương người.
4.3. Kết quả xác định meropenem trong các mẫu thực
Quy trình xử lý mẫu huyết tương đã được tối ưu trong 1 nghiên cứu trước đó của nhóm [18]. Trong đó acetonitrile được sử dụng để tủa và loại bỏ protein, chloroform được sử dụng để chiết Meropenem và tách khỏi các chất phân cực khác có mặt trong mẫu. Do meropenem có tương tác tương đối chọn lọc với CQDs/AuNPs như đã được khảo sát qua độ chọn lọc, nên có thể tiếp tục loại trừ ảnh hưởng của một số chất khác có mặt trong nền mẫu. Kết quả đánh giá khi thêm chuẩn vào mẫu trắng cho thấy mẫu trắng không cho tín hiệu của meropenem, độ thu hồi đạt tương đối cao đạt 83-87% (Bảng 2), đáp ứng yêu cầu của AOAC, chứng minh quy trình xử lý mẫu đã loại bỏ được các ảnh hưởng của nền mẫu và không cần phải khảo sát tối ưu lại các điều kiện ảnh hưởng.
Với kết quả đo mẫu thực, nồng độ meropenem ngay sau khi tiêm là 60,2 ppm, sau 2 h tiêm là 28,4 ppm và sau 5h tiêm nồng độ còn lại trong huyết tương chỉ duy trì ở 6,05 mg/L, có thể thấy nồng độ meropenem giảm dần theo thời gian tiêm truyền. Đáng lưu ý, nồng độ meropenem trong huyết tương của bệnh nhân được quyết định bởi chức năng thận của bệnh nhân, có thể dao động từ 20 mg- 100 mg ngay sau khi tiêm truyền và giảm xuống còn khoảng 2-15 ppm sau 5h tiêm [16, 17]. Qua các kết quả phân tích, có thể kết luận rằng meropenem đã bị đào thải một phần trong quá trình tiêm truyền, nhưng nồng độ còn lại tương đối cao. Điều này chứng tỏ đối tượng mẫu nghiên cứu có chức năng thận hoạt động tốt. Kết quả tương tự đã được chứng minh ở một nghiên cứu khác của nhóm [10, 17]. Sự khác biệt nhỏ (3,5% - 8,1%) giữa kết quả của phương pháp phân tích và phương pháp đối chứng LC-MS/MS cho thấy kết quả của phương pháp huỳnh quang sử dụng vật liệu CQDs/AuNPs là đáng tin cậy.
5. KẾT LUẬN
Nghiên cứu sử dụng thành công phương pháp huỳnh quang trên hệ vật liệu nanocomposite CQDs/AuNPs để định lượng meropenem, và ứng dụng phương pháp để phân tích meropenem trong mẫu huyết tương của bệnh nhân với kết quả đáng tin cậy. Qui trình tổng hợp vật liệu tương đối đơn giản từ các hóa chất cơ bản. Qui trình phân tích có thể dễ dàng thực hiện, giảm thiểu việc sử dụng hóa chất hữu cơ độc hại nhưng vẫn cho kết quả vượt trội so với một số nghiên cứu đã công bố trước đây. Nghiên cứu là một minh chứng cho việc kết hợp vật liệu CQDs và nano vàng vào phân tích y sinh với hiệu quả phân tích cao và chi phí thấp. Các nghiên cứu tiếp theo có thể hướng tới thay đổi nano vàng bằng các nano kim loại khác, mở rộng các đối tượng phân tích cũng như các đối tượng mẫu khác.
Lời cảm ơn: Nghiên cứu này được tiến hành trong khuôn khổ đề tài QG.23.75 của Đại học Quốc gia Hà Nội.
Tuyên bố về sử dụng Gen AI: Các tác giả khẳng định rằng không sử dụng bất kỳ công cụ AI tạo sinh nào để tạo hoặc chỉnh sửa nội dung khoa học của bản thảo này. Mọi phân tích, diễn giải và kết luận hoàn toàn do các tác giả thực hiện.
Tuyên bố về đóng góp của tác giả: Nguyễn Thu Phương: Xây dựng phương pháp nghiên cứu, nghiên cứu, viết bản thảo gốc; Trần Thị Minh Trang: Nghiên cứu, xử lý dữ liệu; Nguyễn Diệu Phương: Nghiên cứu, xử lý dữ liệu, hỗ trợ viết bản thảo; Mạc Hải Nam: Xử lý dữ liệu, chỉnh sửa bản thảo; Nguyễn Tuấn Minh: Xử lý dữ liệu, hỗ trợ chỉnh sửa bản thảo; Vũ Anh Phương: Kiểm định và xác thực kết quả; Đỗ Thị Trang: Kiểm định và xác thực kết quả; Phạm Thị Ngọc Mai: Đề xuất ý tưởng, xây dựng phương pháp nghiên cứu, viết và chỉnh sửa bản thảo.
Tuyên bố về xung đột lợi ích: Không có bất kỳ xung đột lợi ích nào liên quan đến nghiên cứu này.
Tài liệu tham khảo
- L. R. Wiseman, A. J. Wagstaff, R. N. Brogden, and H. M. Bryson, Meropenem: a review of its antibacterial activity, pharmacokinetic properties and clinical efficacy, Drugs, Vol. 50, No. 1, pp. 73-101, 1995.
- T. Armstrong, S. J. Fenn, and K. R. Hardie, JMM Profile: Carbapenems: a broad-spectrum antibiotic, Journal of medical microbiology, Vol. 70, No. 12, p. 001462, 2021.
- A. K. Attia, M. A. Al-Ghobashy, G. M. El-Sayed, and S. M. Kamal, Voltammetric monitoring of linezolid, meropenem and theophylline in plasma, Analytical Biochemistry, Vol. 545, pp. 54-64, 2018.
- Y. Mrestani, R. Neubert, and F. Nagel, Capillary zone electrophoresis determination of meropenem in biological media using a high sensitivity cell, Journal of pharmaceutical and biomedical analysis, Vol. 20, No. 6, pp. 899-903, 1999.
- A. S. Mendez, M. Steppe, and E. E. Schapoval, Validation of HPLC and UV spectrophotometric methods for the determination of meropenem in pharmaceutical dosage form, Journal of pharmaceutical and biomedical analysis, Vol. 33, No. 5, pp. 947-954, 2003.
- C. A. Sutherland and D. P. Nicolau, Development of an HPLC method for the determination of meropenem/vaborbactam in biological and aqueous matrixes, Journal of Chromatographic Science, Vol. 58, No. 8, pp. 726-730, 2020.
- H. Qi et al., Biomass-derived nitrogen-doped carbon quantum dots: highly selective fluorescent probe for detecting Fe3+ ions and tetracyclines, Journal of colloid and interface science, Vol. 539, pp. 332-341, 2019.
- F. Zu et al., The quenching of the fluorescence of carbon dots: a review on mechanisms and applications, Microchimica Acta, Vol. 184, No. 7, pp. 1899-1914, 2017.
- Q. K. Nguyen et al., A highly sensitive fluorescence nanosensor for determination of amikacin antibiotics using composites of carbon quantum dots and gold nanoparticles, Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, Vol. 305, p. 123466, 2024.
- Q. K. Nguyen, M. N. Duong, T. B. Nguyen, and T. N. M. Pham, Visual detection and highly sensitive quantification of antibiotic meropenem in pharmaceutical and human plasma samples using gold nanoparticles, Separation Science and Technology, Vol. 58, No. 8, pp. 1540-1551, 2023.
- E. S. Glazer and S. A. Curley, Non-invasive radiofrequency ablation of malignancies mediated by quantum dots, gold nanoparticles and carbon nanotubes, Therapeutic Delivery, Vol. 2, No. 10, pp. 1325-1330, 2011.
- T. Kitahashi and I. Furuta, Determination of meropenem by capillary electrophoresis using direct injection of serum, Journal of Chromatographic Science, Vol. 43, No. 8, pp. 430-433, 2005.
- S. Asif, T. Alam, A. Nawab, and S. Naveed, Simple UV Spectrophotometric method development for determination of Meropenem in bulk form, RADS Journal of Pharmacy and Pharmaceutical Sciences, Vol. 5, No. 1, pp. 45-49., 2017.
- T. Roth, S. Fiedler, S. Mihai, and H. Parsch, Determination of meropenem levels in human serum by high‐performance liquid chromatography with ultraviolet detection, Biomedical Chromatography, Vol. 31, No. 5, p. e3880, 2017.
- L. Huang, J. Haagensen, D. Verotta, P. Lizak, F. Aweeka, and K. Yang, Determination of meropenem in bacterial media by LC–MS/MS, Journal of Chromatography B, Vol. 961, pp. 71-76, 2014.
- A. Wen et al., Clinical validation of therapeutic drug monitoring of imipenem in spent effluent in critically ill patients receiving continuous renal replacement therapy: a pilot study, PLoS One, Vol. 11, No. 4, p. e0153927, 2016.
- T. N. M. Pham et al., Determination of carbapenem antibiotics using a purpose-made capillary electrophoresis instrument with contactless conductivity detection, Journal of Pharmaceutical and Biomedical Analysis, Vol. 178, p. 112906, 2020. DOI: 10.1016/j.jpba.2019.112906
- Q. K. Nguyen, M. N. Duong, T. B. Nguyen, and T. N. M. Pham, Visual detection and highly sensitive quantification of antibiotic meropenem in pharmaceutical and human plasma samples using gold nanoparticles, Separation Science and Technology, Vol. 58, No. 8, pp. 1540-1551, 2023. DOI: 10.1080/01496395.2023.2189546