Đánh giá tác dụng phục hồi chức năng khứu giác của cao chiết Xuyên Tâm Liên (Andrographis paniculata) trên mô hình chuột bị tổn thương khứu giác bởi methimazole
Viện Y sinh Nhiệt đới, Trung tâm Nhiệt đới Việt - Nga
63 Nguyễn Văn Huyên - Nghĩa Đô - Hà Nội
Số điện thoại: 0987877096; Email: daonguyenmanh0209@gmail.com
Nội dung chính của bài viết
Tóm tắt
Nghiên cứu được thực hiện nhằm đánh giá tác dụng phục hồi chức năng khứu giác của cao chiết Xuyên Tâm Liên (Andrographis paniculata) trên mô hình chuột bị tổn thương biểu mô khứu giác do methimazole gây ra. Cao chiết Xuyên Tâm liên thu được bằng cách chiết hồi lưu với dung môi trích ly EtOH:H2O (8:2, w/w). Chuột nhắt trắng đực, chủng Swiss albino bị gây tổn thương biểu mô khứu giác bằng cách tiêm phúc mạc với methimazole liều 50 mg/kg. Sau khi gây mô hình tổn thương, chuột được điều trị bằng cao chiết Xuyên Tâm Liên (liều uống 150 và 300 mg/kg/ngày) và donepezil (tiêm phúc mạc 1,5 mg/kg/ngày). Từ ngày thứ 7 sau điều trị, tiến hành đánh giá tác dụng phục hồi chức năng khứu giác qua hành vi tìm kiếm mùi, sau khi kết thúc thử nghiệm hành vi thần kinh, tiến hành rửa giải não, tách lớp biểu mô, nhuộm H&E, phân tích mô học biểu mô khứu giác và đo độ dày biểu mô khứu giác. Kết quả cho thấy, cao chiết Xuyên Tâm Liên (liều 150 và 300 mg/kg/ngày) có tác dụng cải thiện chức năng khứu giác bằng thử nghiệm tìm kiếm mùi, giúp rút ngắn thời gian tìm kiếm mùi (p < 0,05), tăng thời gian và số lần chuột ở vùng đích so với nhóm bệnh lý; cải thiện rõ rệt độ dày và cấu trúc biểu mô khứu giác. Kết quả còn cho thấy, ở liều thấp (150 mg/kg) kết quả phục hồi chức năng và biểu mô khứu giác tốt hơn so với ở liều cao (300 mg/kg). Từ những kết quả trên cho thấy, cao chiết Xuyên Tâm Liên có tác dụng phục hồi chức năng khứu giác trên chuột bị tổn thương do methimazole, tác dụng thể hiện rõ hơn ở liều thấp (150 mg/kg).
Abstract
Evaluation of the restorative effects of Andrographis paniculata extract on olfactory function in a methimazole-induced olfactory injury mouse model
The present study aimed to evaluate the olfactory functional recovery effects of an A. paniculata extract in a mouse model of olfactory epithelium injury induced by methimazole. The extract of A. paniculata was obtained by reflux extraction using an EtOH:H₂O solvent mixture in a ratio of 8:2 (w/w). Male Swiss albino mice were induced with olfactory epithelium injury by intraperitoneal injection of methimazole at a dose of 50 mg/kg. Following the induction of injury, the mice were treated with A. paniculata extract at doses of 150 and 300 mg/kg/day and donepezil (1.5 mg/kg/day, intraperitoneally). Beginning on day 7 post-treatment, olfactory function was assessed via odor-finding behavioral tests. Upon completion of behavioral assessments, brain perfusion was performed, followed by olfactory epithelial dissection, hematoxylin and eosin staining, and histological analysis. The results demonstrated that A. paniculata extract at both doses significantly improved olfactory function, as evidenced by a reduction in odor-finding time (p < 0.05), along with increased duration and entries to the target area compared to the pathological control group. Furthermore, marked improvements in the thickness and structural integrity of the olfactory epithelium were observed. Notably, the lower dose (150 mg/kg) yielded more pronounced effects on both functional and histological recovery compared to the higher dose (300 mg/kg). The results suggest that A. paniculata possesses therapeutic potential in promoting the recovery of olfactory function following methimazole-induced epithelial damage in mice, with superior efficacy observed at the lower dosage (150 mg/kg).
Từ khóa
Xuyên Tâm Liên, methimazole, biểu mô khứu giác, mô hình tìm kiếm mùi, mô hình gây tổn thương biểu mô khứu giác bằng methimazole, Andrographis paniculata, olfactory epithelium, odor find test model, methimazole-induced olfactory epithelium injury model
Chi tiết bài viết

Bài báo này được cấp phép theo Creative Commons Attribution 4.0 International License.
- Điểm nổi bật:
Nghiên cứu triển khai mô hình gây tổn thương biểu mô khứu giác bằng methimazole để đánh giá khả năng phục hồi chức năng khứu giác trên động vật thực nghiệm; mô hình này có thể áp dụng để đánh giá hiệu quả phục hồi tổn thương khứu giác do vi rút truyền nhiễm gây ra.
Cải tiến mô hình thử nghiệm tìm kiếm mùi bằng cách thiết kế thêm một hộp nhỏ giúp chuột ổn định trước khi thực hiện hành vi tìm kiếm mùi.
Nghiên cứu đã đánh giá được tác dụng phục hồi chức năng khứu giác của cao chiết Xuyên Tâm Liên trên mô hình chuột methimazole.
1. ĐẶT VẤN ĐỀ
Rối loạn chức năng khứu giác (olfactory dysfunction) là bệnh lý tương đối phổ biến hiện nay với tỷ lệ mắc chứng suy giảm khứu giác ở người trưởng thành lên đến 19% [1, 2]. Tỷ lệ này tăng rõ rệt ở người cao tuổi, với khoảng 25% người trên 50 tuổi và hơn 60% người trên 80 tuổi [3]. Đặc biệt, đại dịch COVID-19 đã làm gia tăng đáng kể tỷ lệ người bị rối loạn chức năng khứu giác. Nghiên cứu của đa trung tâm tại Châu Âu ghi nhận, 85,6% bệnh nhân COVID-19 bị rối loạn khứu giác ở mức độ nhẹ và trung bình, trong đó 79,6% báo cáo mất khứu giác hoàn toàn trong giai đoạn cấp [4]. Mặc dù phần lớn bệnh nhân hồi phục sau vài tuần, tuy nhiên khoảng 10 - 20% bệnh nhân vẫn ghi nhận chứng rối loạn khứu giác kéo dài hơn 6 tháng [4, 5]. Rối loạn chức năng khứu giác không chỉ làm giảm khả năng nhận biết mùi mà còn ảnh hưởng sâu sắc tới chất lượng sống, làm suy giảm vị giác, tăng nguy cơ rối loạn ăn uống, tăng tỷ lệ trầm cảm, lo âu và giảm tương tác xã hội [6, 7].
Biểu mô khứu giác là lớp mô thần kinh đặc biệt nằm ở vùng trần mũi, gồm các tế bào thần kinh khứu giác (ORNs), tế bào nâng đỡ và tế bào đáy. ORNs đảm nhiệm tiếp nhận và dẫn truyền tín hiệu mùi, tế bào nâng đỡ bảo vệ môi trường vi mô, còn tế bào đáy cơ bản chịu trách nhiệm tái tạo các tế bào thần kinh mới [8, 9]. Đặc điểm nổi bật của biểu mô khứu giác là khả năng tái sinh suốt đời, một cơ chế rất hiếm trong hệ thần kinh trưởng thành. Sau tổn thương do virus, viêm hoặc hóa chất, các tế bào đáy có thể biệt hóa thành neuron mới giúp phục hồi chức năng khứu giác [10, 11]. Tuy nhiên, quá trình tái sinh này bị giới hạn bởi tuổi tác, mức độ viêm, stress oxy hóa và sự mất cân bằng các yếu tố tăng trưởng thần kinh [12].
Xuyên Tâm Liên (Andrographis paniculata) là dược liệu truyền thống phổ biến tại Châu Á, với hoạt chất chính là andrographolide, đây là diterpenoid đã được nhiều nghiên cứu quốc tế xác nhận có phổ tác dụng dược lý rộng [13]. Một số nghiên cứu cho thấy tác dụng chống viêm mạnh mẽ của Xuyên Tâm Liên thông qua ức chế các cytokine như TNF-α, IL-1β, IL-6, đồng thời ức chế hoạt hóa NF-κB, giảm các phản ứng viêm mạn tính [14, 15]. Tác dụng chống oxy hóa của dược liệu này cũng được chứng minh thông qua khả năng tăng hoạt động các enzyme chống oxy hóa nội sinh (SOD, catalase, glutathione peroxidase), giúp bảo vệ tế bào thần kinh khỏi tổn thương do stress oxy hóa [16, 17].
Đáng chú ý, một số nghiên cứu gần đây cho thấy tác dụng bảo vệ và tái tạo thần kinh của andrographolide và các dẫn chất, thể hiện qua tăng biểu hiện các yếu tố tăng trưởng thần kinh (NGF, BDNF), giảm apoptosis, thúc đẩy tái tạo thần kinh trên mô hình tổn thương thần kinh ngoại vi và trung ương [18-20]. Ngoài ra, Xuyên Tâm Liên còn có tác dụng kháng khuẩn, kháng virus và hỗ trợ điều trị các bệnh viêm đường hô hấp, viêm mũi xoang - những yếu tố nguy cơ thường gặp của rối loạn khứu giác. Một số thử nghiệm lâm sàng cho thấy chiết xuất Xuyên Tâm Liên an toàn, dung nạp tốt và có hiệu quả trong giảm triệu chứng, rút ngắn thời gian mắc các bệnh lý viêm nhiễm [21-24]. Nhờ phổ tác dụng chống viêm, chống oxy hóa, bảo vệ và tái sinh thần kinh, cùng khả năng điều hòa miễn dịch và kháng khuẩn, Xuyên Tâm Liên có thể là dược liệu tiềm năng hỗ trợ phục hồi chức năng khứu giác. Nghiên cứu nhằm đánh giá, làm rõ tác dụng cải thiện chức năng khứu giác của dược liệu này trên mô hình động vật thực nghiệm.
2. NGUYÊN VẬT LIỆU VÀ PHƯƠNG PHÁP NGHIÊN CỨU
2.1. Vật liệu nghiên cứu
Xuyên Tâm Liên do Công ty Dược liệu Indochina cung cấp, sau khi loại tạp, tiến hành sấy khô ở 50oC cho đến khi độ ẩm ≤ 10%, sau đó nghiền nhỏ. Tiến hành chiết với dung môi trích ly EtOH:H2O (8:2, w/w), tỷ lệ dung môi/dược liệu là 1:10 (w/w) ở nhiệt độ 65 oC trong 4 h bằng thiết bị chiết Soxhlet. Lọc lấy dịch chiết, cặn tiếp tục chiết lặp lại với dung môi và điều kiện như trên, sau đó gộp dịch chiết và cô chân không ở nhiệt độ 60oC để thu hồi cao khô. Hiệu suất thu hồi cao khô 10,41% (w/w).
Hàm lượng của andrographolide trong mẫu cao chiết được xác định bằng phương pháp HPLC với điều kiện như sau: Cột sắc ký C18 5 µm (4,6 x 250 mm); detector PDA, bước sóng cực đại 223 nm; nhiệt độ cột 25℃; thể tích tiêm 10 µL; pha động ACN/H3PO4 0,1% (65/35); tốc độ dòng 0,8 mL/phút. Pha dung dịch chuẩn andrographolide thành các dải nồng độ khác nhau, xây dựng phương trình hồi quy tuyến tính biểu thị sự tương quan giữa diện tích píc và nồng độ các dung dịch chuẩn (hình 1).
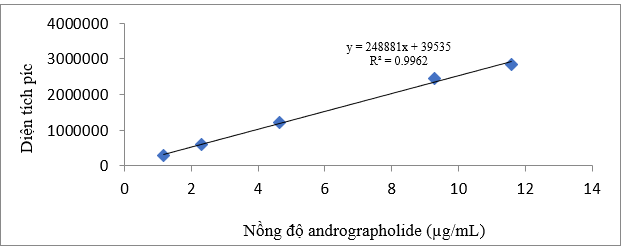
Hình 1. Biểu đồ tương quan tuyến tính giữa nồng độ dung dịch chuẩn và diện tích píc
Pha dung dịch cao trong methanol thu được nồng độ dung dịch 0,1 mg/mL, chạy HPLC với chương trình như trên, kết quả thu được ở hình 2.
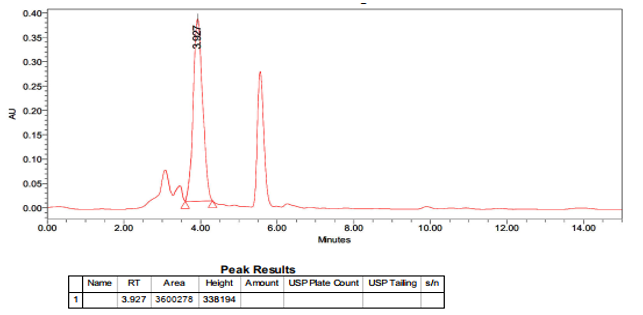
Hình 2. Sắc ký đồ của mẫu cao chiết Xuyên Tâm Liên
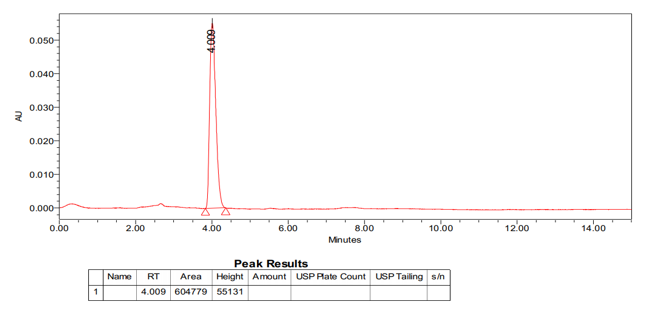
Hình 3. Sắc ký đồ mẫu chuẩn andrographolide
Từ diện tích píc của mẫu cao chiết, xác định được hàm lượng trung bình của andrographolide trong dược liệu khô là 1,4% (w/w) (hình 3).
2.2. Động vật sử dụng trong nghiên cứu
Động vật sử dụng trong nghiên cứu là chuột nhắt trắng chủng Swiss albino, giống đực, khỏe mạnh, cân nặng trung bình 20 - 30 g được cung cấp bởi Viện Vệ sinh dịch tễ Trung ương. Chuột được nuôi ổn định trong điều kiện phòng nuôi động vật thí nghiệm với nhiệt độ trung bình khoảng 22oC, chu kỳ sáng tối 12/12 h, được ăn thức ăn theo tiêu chuẩn dành cho động vật nghiên cứu, uống nước tự do. Chuột được nuôi ổn định 7 ngày trước khi tiền hành thử nghiệm.
2.3. Phương pháp nghiên cứu
* Sơ đồ nghiên cứu: Hình 4.
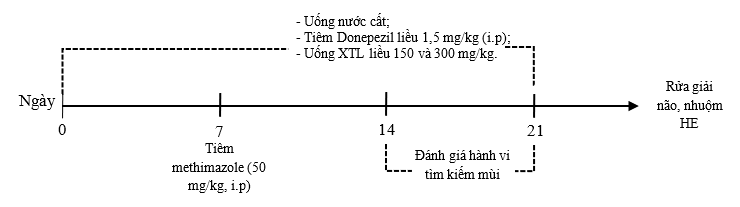
Hình 4. Sơ đồ nghiên cứu
* Phương pháp nghiên cứu
Nghiên cứu tiến hành đánh giá tác dụng cải thiện chức năng khứu giác của Xuyên Tâm Liên trên mô hình chuột bị tổn thương biểu mô khứu giác bằng methimazole. Chuột được điều trị một tuần trước khi gây mô hình tổn thương biểu mô khứu giác. Sau khi gây mô hình, tiếp tục điều trị 01 tuần sau đó tiến hành đánh giá tác dụng cải thiện chức năng khứu giác bằng mô hình tìm kiếm mùi bơ lạc, kết thúc thử nghiệm hành vi tiến hành rửa giải não, nhuộm H&E để kiểm tra mức độ tổn thương và độ dày biểu mô khứu giác. Chuột được nhịn đói 24 h trước khi tập và chỉ uống nước. Vào ngày tiến hành các bài tập hành vi, chuột được uống nước, cao chiết hoặc tiêm donepezil 60 phút trước khi tập. Chuột thử nghiệm được chia thành 05 nhóm, mỗi nhóm từ 10-12 con, cụ thể:
- Nhóm chứng sinh lý: Không tiêm methimazole, uống nước cất (0,1 mL/10g/ngày) trong suốt quá trình thử nghiệm.
- Nhóm bệnh lý: Chuột được tiêm phúc mạc bằng methimazole với liều 50 mg/kg. Sau đó uống nước cất (0,1 mL/10g/ngày) trong suốt quá trình thử nghiệm.
- Các nhóm điều trị bằng cao chiết Xuyên Tâm Liên: Chuột được tiêm phúc mạc bằng methimazole với liều 50 mg/kg. Sau đó được điều trị bằng Xuyên Tâm Liên với liều 150 và 300 mg/kg hằng ngày.
- Nhóm đối chứng: Chuột được tiêm phúc mạc bằng methimazole với liều 50 mg/kg, sau đó điều trị bằng donepezil với liều 1,5 mg/kg/ngày (tiêm phúc mạc).
Cao chiết Xuyên Tâm Liên được pha trong dung dịch CMC 0,5% với tỷ lệ 150 mg trong 10 mL hoặc 300 mg trong 10 mL tương ứng với liều 150 mg/kg và 300 mg/kg.
2.3.1. Mô hình tìm kiếm mùi (OFT) [25, 26]
Thử nghiệm được tiến hành trong hộp gỗ B (kích thước, dài x rộng x cao: 40 x 20 x 20 cm) với chất độn trong chuồng có độ sâu 5 cm. Mô hình bao gồm hộp gỗ A (kích thước, dài x rộng x cao: 10 x 10 x 20) thông với hộp gỗ B, cách nhau bằng một cửa kéo lùa lên trên. Việc thiết kế thêm hộp gỗ A giúp chuột ổn định tinh thần, tránh tác động của thao tác đến hành vi tìm kiếm mùi (hình 5).
Thử nghiệm được tiến hành theo 02 giai đoạn: Giai đoạn thử nghiệm và kiểm tra. Ở tất cả giai đoạn, mỗi bài tập đều sử dụng tấm giấy lọc (kích thước: 4 x 4 cm) tẩm bơ lạc với nồng độ 1,2 g/mL được vùi dưới chất độn (tại vị trí C), vị trí đặt là ở trung tâm trong các cung phần tư của mỗi bài kiểm tra để ngăn chặn tất cả các yếu tố ngẫu nhiên chuột có thể tìm thấy thức ăn. Sau khi kết thúc bài tập, tiến hành thay giấy lọc tẩm bơ lạc, làm sạch vị trí đặt giấy lọc tẩm bơ lạc bằng cồn, quạt cho bay mùi bơ lạc trong khu vực thử nghiệm hành vi.

Hình 5. Mô hình tìm kiếm mùi
- Giai đoạn tập luyện: Ở giai đoạn này chuột được đưa vào khu A để tránh sợ hãi, ổn định tâm lý, sau đó mở cửa để chuột di chuyển tự do trong hộp B 10 phút để tìm giấy tẩm bơ lạc ở vị trí C và làm quen với không gian. Sau đó chuột được đưa ra chuồng để nghỉ trong vòng 5 phút. Giai đoạn này mỗi con chuột được tập luyện 3 lần.
- Giai đoạn kiểm tra: Sau khi kết thức tập luyện, tiến hành kiểm tra hành vi tìm kiếm mùi của chuột với phương thức tương tự như lúc tập luyện, chỉ khác về thời gian kiểm tra là 180 giây. Camera và phần mềm ANY-maze (Mỹ) ghi lại di chuyển của chuột khi đi vào khu vực B, đồng thời ghi lại thời gian chuột tìm thấy giấy tẩm bơ lạc tại C. Nếu chuột không tìm thấy tấm giấy tẩm bơ lạc trong 180 giây này thì thử nghiệm được coi là hoàn thành ở 180 giây.
2.3.2. Phương pháp nhuộm hóa mô H&E và đo độ dày biểu mô
Chuột được gây mê bằng chloral hydrate (50 mg/kg, i.p). Sau khi chuột gây mê hoàn toàn, tiến hành rửa giải não chuột bằng nước muối 0,9%, tách đầu chuột (bao gồm cả não và mũi). Mẫu được hủy xương bằng cách ngâm trong dung dịch 0,5M EDTA pH 8,0 trong một tuần ở 4oC. Sau khi hủy xương, mẫu tiếp tục được cố định trong paraformaldehyde 4% ít nhất trong 2 h.Mẫu được gửi tới Bệnh viện Trung ương Quân đội 108 để tiếp tục xử lý các bước tiếp theo: đúc parafin, cắt tiêu bản.
Tiêu bản được cắt bằng thiết bị cắt tiêu bản HM 325 (Thermo Scientific) với độ dày 5 µm, mỗi mẫu cắt 02 tiêu bản, vị trí cắt được mô tả tại hình 6.
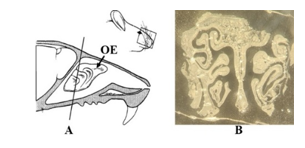
Hình 6. Vị trí cắt tiêu bản (A: Vị trí lát cắt tiêu bản; B: Tiêu bản đúc parafin sau khi cắt (2X))
Sau đó, tiêu bản mũi chuột sẽ được nhuộm H&E, quy trình nhuộm H&E được mô tả tóm tắt như sau: Tẩy parafin trong 03 bể xylen, mỗi bể 5 phút; nhúng qua 4 bể cồn: 100% - 95% - 80% - 70%, mỗi bể 15 giây. Sau đó rửa bằng nước cất (nhúng trong bể 15 giây); nhuộm nhân bằng Hematoxylin Harris trong 6 phút, sau đó rửa dưới vòi nước chảy 10 phút, kiểm tra màu của nhân qua kính hiển vi; nhuộm Eosin 0,1% (Eosin B) trực tiếp 1-2 phút, sau đó rửa dưới vòi nước chảy 1 phút. Loại bỏ phẩm nhuộm thừa bằng cồn 95% - 100%, mỗi chặng 5-10 giây; tẩy cồn bằng xylen: 3 chặng, mỗi chặng 5-10 giây, sau đó gắn lamen.
Biểu mô chuột được đọc và đo độ dày biểu mô bằng phần mềm trên máy vi tính kết nối trực tiếp với kính hiển vi soi ngược huỳnh quang phản pha Olympus IX73 (vật kính 10X). Đo ở 8 vị trí khác nhau trên một tiêu bản mũi chuột, lấy kết quả trung bình để xác định độ dày biểu mô. Vị trí đo độ dày biểu mô được mô tả tại hình 7.
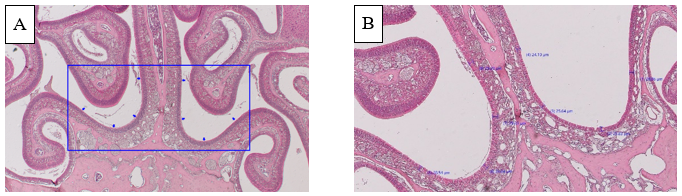
Hình 7. Vị trí đo độ dày biểu mô
(A: Các vị trí đo độ dày biểu mô; B: Đo độ dày bằng phần mềm kết nối trực tiếp với kính hiển vi Olympus IX73, 10X)
2.3.3. Phương pháp phân tích số liệu
Số liệu được xử lý thống kê bằng phần mềm SPSS 27. Dữ liệu được biểu thị dưới dạng Mean ± SE (Mean: giá trị trung bình, SE: sai số chuẩn). Sử dụng kiểm định ANOVA kèm hậu kiểm Tukey để so sánh sự khác biệt giữa các lô nghiên cứu. Sự khác biệt được coi là có ý nghĩa thống kê khi p < 0,05.
2.3.4. Đạo đức trong nghiên cứu
Nghiên cứu tuân thủ đầy đủ các quy định về đạo đức trong nghiên cứu trên động vật. Động vật thí nghiệm được chăm sóc trong điều kiện chuồng trại đúng quy định, được cung cấp thức ăn và nước uống theo tiêu chuẩn.
3. KẾT QUẢ
3.1. Kết quả phục hồi chức năng khứu giác trên mô hình tìm kiếm mùi
Thử nghiệm OFT nhằm đánh giá khả năng khứu giác của động vật thí nghiệm thông qua hình vi đi tìm mùi thơm của bơ lạc. Chuột là động vật có khứu giác rất nhạy bén, sau khi để đói 24 h, chúng sẽ có xu hướng đi tìm kiếm thức ăn khi thả tự do trong buồng. Thử nghiệm tiến hành đánh giá các chỉ số về thời gian chuột tìm thấy thức ăn, thời gian và số lần chuột ở vùng đích (vùng có thức ăn) để xác định mức độ phục hồi chức năng khứu giác. Kết quả được thể hiện qua hình 8 và hình 9.
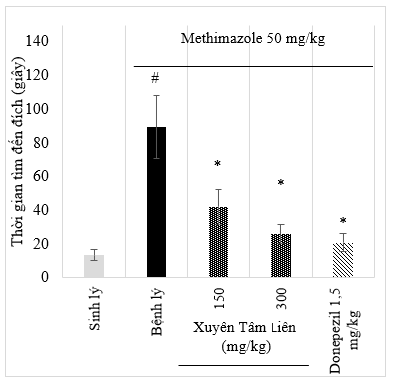
Hình 8. Thời gian tìm đến đích (thức ăn) của các nhóm
(Số liệu được biểu diễn dưới dạng Mean ± SE, trong đó: #: P < 0,001 khi so sánh với nhóm sinh lý, *: p < 0,05 khi so sánh với nhóm bệnh lý)
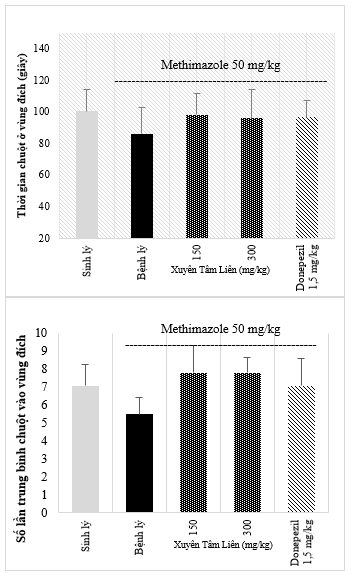
Hình 9. Thời gian và số lần ở vùng đích của các nhóm
Kết quả ở hình 8 cho thấy, thời gian tìm kiếm đến đích của các nhóm sinh lý, nhóm điều trị bằng cao chiết Xuyên Tâm Liên, donepezil thấp hơn rất nhiều so với nhóm bệnh lý. Trong đó, nhóm sinh lý và bệnh lý có sự khác biệt rất rõ ràng (p < 0,001), điều này cho thấy thử nghiệm OFT là phù hợp để đánh giá tác dụng cải thiện chức năng khứu giác trên mô hình chuột methimazole. Chuột điều trị bằng cao chiết Xuyên Tâm Liên (liều 150 và 300 mg/kg) đều có thời gian tìm kiếm đến đích thấp hơn so với nhóm bệnh lý (p < 0,05). Ở nhóm được điều trị bằng donepezil liều 1,5 mg/kg có thời gian tìm đến đích cũng ngắn hơn so với nhóm chuột bệnh lý (p < 0,05). Như vậy, cao chiết Xuyên Tâm Liên (150 và 300 mg/kg) có tác dụng trong cải thiện chức năng khứu giác của chuột methimazole.
Tác dụng cải thiện chức năng khứu giác còn thể hiện qua hành vi đi tìm thức ăn thông qua thời gian và số lần chuột vào vùng đích (vùng có thức ăn). Ở hình 9 cho thấy, chuột ở nhóm bệnh lý có thời gian và số lần vào vùng đích ít hơn tương đối so với chuột ở các nhóm sinh lý và nhóm được điều trị. Điều này cho thấy, chức năng khứu giác của chuột đã được phục hồi, chuột có xu hướng vận động nhiều ở khu vực có mùi thức ăn để tìm kiếm và ăn.
3.2. Kết quả đo độ dày biểu mô khứu giác
Độ dày và hình ảnh giải phẫu mô hiểu học của biểu mô khứu giác phản ánh rõ rệt mức độ phục hồi chức năng khứu giác ở chuột methimazole. Kết quả được thể hiện ở hình 10 và hình 11.
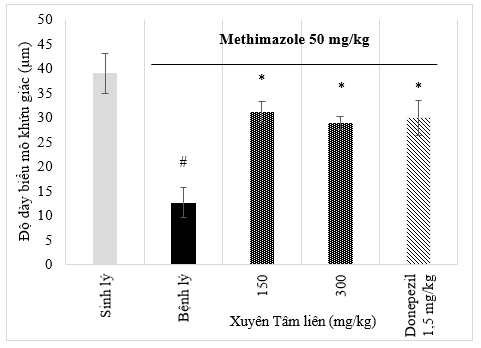
Hình 10. Độ dày biểu mô khứu giác
(Số liệu được biểu diễn dưới dạng Mean ± SE, trong đó: #: P < 0,001 khi so sánh với nhóm sinh lý, *: tương ứng với p < 0,01 khi so sánh với nhóm bệnh lý)
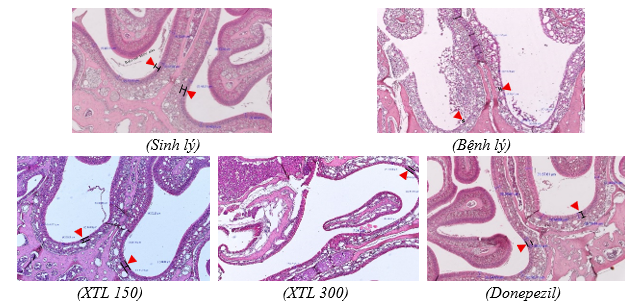
Hình 11. Hình ảnh giải phẫu mô học biểu mô khứu giác (Ảnh chụp ở vật kính 10X)
Kết quả đo độ dày lớp biểu mô khứu giác cho thấy, chuột ở nhóm bệnh lý có lớp biểu mô mỏng hơn rất nhiều so với chuột ở nhóm sinh lý, sự khác biệt có ý nghĩa thống kê ( p < 0,001). Ở các nhóm được điều trị bằng Xuyên Tâm Liên và Donepezil, lớp biểu mô đều dày hơn nhóm bệnh lý (p < 0,01, sự khác biệt có ý nghĩa thống kê) và tương đương với nhóm sinh lý. Quan sát đặc điểm hình thái mô học biểu mô khứu giác chuột cho thấy: chuột ở lô sinh lý có lớp tế bào biểu mô khứu giác dày, xếp đều đặn, trong khi đó chuột ở lô bệnh lý có lớp tế bào biểu mô rất mỏng, xếp lỏng lẻo, đôi khi có hiện tượng rách trong lớp này; ở các nhóm XTL150, XTL300 và Donepezil, có sự phục hồi rõ rệt ở lớp biểu mô, trong đó nhóm chuột donepezil có nhu mô đều, dày gần tương đồng với nhóm sinh lý.
4. THẢO LUẬN
Methimazole là một thuốc kháng giáp thường được ứng dụng rộng rãi trong nghiên cứu tiền lâm sàng nhằm xây dựng các mô hình mất chức năng khứu giác trên động vật thực nghiệm. Đây là một hợp chất độc đặc hiệu trên biểu mô khứu giác. Khi đưa vào cơ thể động vật, điển hình là qua đường tiêm phúc mạc hoặc nhỏ mũi, sẽ làm tổn thương chọn lọc vào tế bào biểu mô cảm nhận mùi, gây suy giảm hoặc mất chức năng khứu giác tạm thời [27, 28]. Quá trình hồi phục chức năng khứu giác sau tổn thương được ứng dụng để đánh giá hiệu quả điều trị của các thuốc hoặc liệu pháp can thiệp mới thông qua các nghiên cứu như phục hồi hành vi khứu giác và tái tạo mô học [29]. Trong nghiên cứu này, chúng tôi đã sử dụng methimazole với liều 50 mg/kg để làm chất độc gây tổn thương biểu mô khứu giác nhằm đánh giá tác dụng phục hồi chức năng khứu giác của cao chiết Xuyên Tâm Liên.
Thử nghiệm về độc tính cấp của cao chiết chuẩn Xuyên Tâm Liên theo hướng dẫn của OECD với liều duy nhất 5000 mg/kg cho thấy, không xác định được LD50 và biểu hiện độc tính trên chuột sau 14 ngày uống cao chiết [30]. Trước khi gây mô hình tổn thương biểu mô khứu giác, chuột được uống cao chiết Xuyên Tâm Liên trong vòng 7 ngày, theo dõi tình trạng chung cho thấy, các nhóm chuột đều ăn tốt, vận động linh hoạt. Cao chiết Xuyên Tâm Liên không làm ảnh hưởng đến vị giác và chức năng vận động của các nhóm chuột nghiên cứu.
Quá trình thử nghiệm hành vi chịu tác động của nhiều yếu tố như mùi thức ăn, tình trạng chuột, tác động của ngoại cảnh và thao tác. Trong nghiên cứu này chúng tôi sử dụng bơ lạc là chất tạo mùi, kích thích khứu giác của chuột. Tương tự như các nghiên cứu, chuột được nhịn đói 24h để tạo động lực tìm kiếm thức ăn, ở giai đoạn luyện tập chuột được tìm thức ăn trong đồng thời khám phá không gian 30 phút, giúp giảm bớt nhiễu do xu hướng khám phá không gian thay vì tìm kiếm thức ăn [25, 26]. Thực tế cho thấy, ở nhóm bệnh lý có một vài con mặc dù bị bỏ đói 24h nhưng do tổn thương khứu giác nên không thể phát hiện ra mùi thức ăn và không thể tìm được thức ăn trong 180 giây.
Thao tác đưa chuột vào trong hộp mô hình cũng ảnh hưởng rất nhiều đến kết quả, quá trình chuyển chuột từ chuồng vào trong hộp thử nghiệm có thể khiến cho chuột sợ và chạy thẳng đến vị trí đích, kết quả không phản ánh đúng hành vi tìm kiếm mùi của chuột. Để giải quyết vấn đề trên, nhóm nghiên cứu đã cải tiến mô hình nghiên cứu bằng cách thiết kế thêm một hộp A nối liền với hộp thử nghiệm hành vi (Hình 2). Chuột được đưa vào hộp A để ổn định tâm lý, đảm bảo không còn sợ hãi, sau đó mới mở cửa để chuột dựa theo mùi đi tìm kiếm thức ăn tại vị trí C.
Việc phục hồi chức năng khứu giác ở chuột methimazole phụ thuộc vào nhiều yếu tố, trong đó cơ chế quan trọng nhất có thể là nhờ vào sự tái tạo tế bào thần kinh thụ cảm khứu giác nhờ quá trình tăng sinh và biệt hóa của tế bào đáy (HBC, GBC). Đồng thời quá trình phục hồi còn phụ thuộc các yếu tố tác động đến như quá trình oxy hóa, stress oxy hóa gây tổn thương tế bào. Bản thân methimazole không gây độc cho biểu mô khứu giác, mà chất chuyển hóa trung gian được hoạt hóa bởi các enzyme monooxygenase là nguyên nhân chính gây ra độc biểu mô khứu giác [31]. Xuyên Tâm Liên đã được minh chứng có tác dụng chống oxy hóa và giảm tổn thương do stress oxy hóa gây ra [16, 17], đồng thời andrographolide và các dẫn xuất flavonoid có khả năng kích thích các yếu tố tăng trưởng như: EGF (yếu tố tăng trưởng biểu bì - Epidermal Growth Factor) và NGF (yếu tố tăng trưởng thần kinh - Nerve Growth Factor), từ đó thúc đẩy quá trình tăng sinh, biệt hóa và tái tạo tế bào biểu mô khứu giác mới. Điều này góp phần lý giải được khả năng phục hồi chức năng khứu giác của Xuyên Tâm Liên trong nghiên cứu của chúng tôi [32]. Ở mô hình tìm kiếm mùi, sau khi được điều trị bằng Xuyên Tâm Liên, đa số chuột đều có cảm nhận mùi rõ rệt thể hiện qua hành vi đi tìm kiếm thức ăn và ăn; kết quả phục hồi biểu mô khứu giác cũng thể hiện rõ rệt so với nhóm bệnh lý.
Trong nghiên cứu này, chúng tôi sử dụng donepezil như đối chứng dương. Donepezil là một chất ức chế acetylcholinesterase, được sử dụng phổ biến trong điều trị bệnh Alzheimer nhằm tăng cường tín hiệu cholinergic trong não. Gần đây, nhiều nghiên cứu cho thấy donepezil (liều tiêm 1-3 mg/kg), không chỉ cải thiện chức năng nhận thức mà còn cả chức năng cảm giác khứu giác, đặc biệt trong các mô hình chuột bị tổn thương hành khứu (olfactory bulbectomy). Donepezil phục hồi chức năng khứu giác thông qua kích thích tăng sinh tế bào thần kinh ở hành khứu và giảm stress oxy hóa [33-35]. Kết quả nghiên cứu cũng minh chứng cho thấy hiệu quả cải thiện chức năng và phục hồi biểu mô khứu giác của donepezil ở chuột methimazole. So sánh với nhóm điều trị bằng donepezil, cao chiết Xuyên Tâm Liên đều cho thấy hiệu quả tương đồng, thậm trí còn tốt hơn với liều thấp (150 mg/kg). Kết quả nghiên cứu phần nào minh chứng cho tác dụng của Xuyên Tâm Liên đối với cải thiện chức năng khứu giác ở chuột methimazole.
Đánh giá về tác dụng phục hồi chức năng khứu giác ở nhóm chuột điều trị bằng Xuyên Tâm Liên qua kết quả đo độ bày biểu mô khứu giác và hình ảnh giải phẫu biểu mô học cũng cho thấy, liều 150 mg/kg cho hiệu quả tốt hơn so với liều 300 mg/kg. Hiện tượng này có thể được giải thích thông qua khái niệm về Hormesis – hiện tượng sinh học mà một chất ở nồng độ thấp mang lại hiệu ứng có lợi, nhưng khi tăng liều thì hiệu quả giảm hoặc thậm chí gây độc. Cơ chế trên về giả thuyết có thể được giải thích như sau: Ở liều thấp andrographolide và dẫn chất kích thích nhẹ quá trình đáp ứng thích nghi, bao gồm kích hoạt vừa đủ các yếu tố bảo vệ thần kinh (NGF, BDNF), giảm nhẹ phản ứng viêm nhưng không ức chế hoàn toàn quá trình phục hồi tự nhiên. Cơ chế điều hòa miễn dịch được cân bằng nhẹ nhàng, không bị ức chế quá mức, giúp cơ thể tăng khả năng tự phục hồi. Tuy nhiên, khi ở liều cao andrographolide và các dẫn chất có thể gây ức chế quá mức các phản ứng viêm cần thiết trong giai đoạn đầu tái tạo mô, làm giảm các cytokine bảo vệ và các yếu tố tăng trưởng tự nhiên cần thiết. Kích thích quá mức các enzyme chống oxy hóa nội sinh, có thể dẫn đến mất cân bằng oxy hóa-khử, làm chậm quá trình hồi phục tế bào thần kinh. Liều cao có thể gây stress tế bào hoặc ngộ độc tế bào thần kinh nhẹ, làm giảm hiệu quả tái sinh tế bào thần kinh khứu giác [36, 37].
Xuyên Tâm Liên qua nghiên cứu đã chứng minh có hiệu quả phục hồi tổn thương khứu giác, tuy nhiên việc sử dụng Xuyên Tâm Liên ở liều thấp hoặc vừa đủ sẽ tối ưu hóa hiệu quả điều trị và tránh tác dụng phụ hoặc giảm hiệu quả do dùng liều cao không cần thiết. Điều này nhấn mạnh tầm quan trọng của việc xác định chính xác liều tối ưu khi sử dụng thảo dược này trong điều trị các tổn thương liên quan đến thần kinh.
Nghiên cứu sử dụng mô hình gây tổn thương biểu mô khứu giác bằng methimazole giúp đánh giá khả năng phục hồi chức năng khứu giác một cách thuận tiện và có chi phí thấp. Tuy nhiên, tổn thương chủ yếu ở lớp biểu mô ngoại biên, nên chưa phản ánh đầy đủ cơ chế viêm và thoái hóa thần kinh như ở người. Ngoài ra, methimazole là thuốc kháng giáp, có thể ảnh hưởng đến chuyển hóa toàn thân và hành vi, gây nhiễu trong các thử nghiệm hành vi. Nghiên cứu chỉ dừng lại ở nhộm hóa mô H&E để đánh giá mức độ phục hồi tổng thể ở biểu mô khứu giác của chuột, chưa thực hiện nhuộm hóa mô miễn dịch với các marker như OMP, Ki67 để minh chứng rõ hơn về sự tái tạo của các tế bào thần kinh cảm thụ khứu giác. Vì thế, cần tiếp tục thực hiện các nghiên cứu sâu để đưa ra các minh chứng về cơ chế phục hồi tổn thương khứu giác của Xuyên Tâm Liên.
5. KẾT LUẬN
Nghiên cứu đã chứng minh, cao chiết ethanol của Xuyên Tâm Liên (Andrographis paniculata) với liều 150 mg/kg có tác dụng phục hồi chức năng khứu giác rõ rệt trên mô hình gây tổn thương bằng methimazole, thể hiện cả trên hành vi tìm kiếm mùi và phục hồi cấu trúc mô học. Việc sử dụng Xuyên Tâm Liên với liều hợp lý có tiềm năng trong hỗ trợ điều trị rối loạn khứu giác, nhất là trong bối cảnh các bệnh lý gây mất khứu giác ngày càng gia tăng.
Lời cảm ơn: Bài báo nằm trong khuôn khổ đề tài cấp cơ sở của Trung tâm Nhiệt đới Việt - Nga: «Nghiên cứu đánh giá tác dụng phục hồi hành vi thần kinh và tổn thương tế bào khứu giác của cao chiết, hoạt chất tinh sạch trong một số dược liệu ở Việt Nam» với sự tham gia giúp đỡ của Khoa Dược lý - Sinh hóa thuộc Viện Dược liệu/Bộ Y tế.
Tuyên bố về sử dụng Gen AI: Các tác giả khẳng định rằng không sử dụng bất kỳ công cụ AI tạo sinh nào để tạo hoặc chỉnh sửa nội dung khoa học của bản thảo này. Mọi phân tích, diễn giải và kết luận hoàn toàn do các tác giả thực hiện.
Tuyên bố về đóng góp của tác giả: Đào Nguyên Mạnh: Xây dựng tổng quan, soạn bản thảo bài báo; Võ Viết Cường, Phạm Thị Nguyệt Hằng: Rà soát, hiệu đính các mô hình nghiên cứu và chịu trách nhiệm nội dung bản thảo; Bùi Thị Hương, Quách Thị Quỳnh, Phí Đình Uy: Tham gia thực hiện nghiên cứu trên mô hình tìm kiếm mùi và nhuộm hóa mô H&E, tổng hợp số liệu; Trần Thanh Tuấn: Xử lý số liệu.
Tuyên bố về xung đột lợi ích: Nhóm tác giả cam kết không có bất cứ xung đột lợi ích nào trong nghiên cứu.
Tài liệu tham khảo
- Hummel et al., Position paper on olfactory dysfunction, Rhinology Supplement, Vol. 54, No. 26, pp. 1-30, 2017. DOI: 10.4193/Rhino16.248
- Brämerson, L. Johansson, L. Ek, S. Nordin and M. Bende, Prevalence of olfactory dysfunction: The Skövde population-based study, The Laryngoscope, Vol. 114, No. 4, pp. 733-737, 2004. DOI: 10.1097/00005537-200404000-00026
- L. Doty, V. Kamath, The influences of age on olfaction: A review, Frontiers in Psychology, Vol. 5, No. 20, 2014. DOI: 10.3389/fpsyg.2014.00020
- R. Lechien et al., Olfactory and gustatory dysfunctions as a clinical presentation of mild‐to‐moderate forms of the coronavirus disease (COVID‐19): A multicenter European study, Eur Arch Otorhinolaryngol, Vol. 277, No. 8, pp. 2251-2261, 2020. DOI: 10.1007/s00405-020-05965-1
- Boscolo-Rizzo et al., High prevalence of long-term olfactory, gustatory, and chemesthesis dysfunction in post-COVID-19 patients: a matched case-control study with one-year follow-up using a comprehensive psychophysical evaluation, Rhinology, Vol. 59, No. 6, pp. 517-527, 2021. DOI: 10.4193/Rhin21.249
- Oleszkiewicz et al., Quality of life in patients with olfactory loss is better predicted by flavor identification than by orthonasal olfactory function, Chemical senses, Vol. 44, No. 6, pp. 371-377, 2019. DOI: 10.1093/chemse/bjz027
- Kohli, Z. M. Soler, S. A. Nguyen, J. S. Muus and R. J. Schlosser, The association between olfaction and depression: A systematic review, Chemical Senses, Vol. 41, No. 6, pp. 479-486, 2016. DOI: 10.1093/chemse/bjw061
- H. Brann, S. J. Firestein, A lifetime of neurogenesis in the olfactory system, Frontiers in Neuroscience, Vol. 8, No. 182, 2014. DOI: 10.3389/fnins.2014.00182
- E. Schwob, Neural regeneration and the peripheral olfactory system, The Anatomical Record, Vol. 269, No. 1, pp. 33-49, 2002. DOI: 10.1002/ar.10047
- A. Durante et al., Single-cell analysis of olfactory neurogenesis and differentiation in adult humans, Nature Neuroscience, Vol. 23, No. 3, pp. 323-326, 2020. DOI: 10.1038/s41593-020-0587-9
- M. Child, D. B. Herrick, J. E. Schwob, E. H. Holbrook and W. Jang, The neuroregenerative capacity of olfactory stem cells is not limitless: Implications for aging, J Neurosci, Vol. 38, No. 31, pp. 6806-6824, 2018. DOI: 10.1523/JNEUROSCI.3261-17.2018
- Matarazzo, F. Muscatello, L. Munari and D. Polese, Mechanisms of olfactory dysfunction and therapeutic strategies, Current Pharmaceutical Design, Vol. 26, No. 17, pp. 1989-2000, 2020. doi: 10.1186/s40001-025-02740-y
- Akbar, Andrographis paniculata: A review of pharmacological activities and clinical effects, Alternative medicine review: a Journal of Clinical Therapeutic, Vol. 16, No. 1, pp. 66-77, 2011.
- A. Abu-Ghefreh, H. Canatan and C. I. Ezeamuzie, In vitro and in vivo anti-inflammatory effects of andrographolide, International Immunopharmacology, Vol. 9, No. 3, pp. 313-318, 2009. DOI: 10.1016/j.intimp.2008.12.002
- C. Lim, T. K. Chan, D. S. Ng, S. R. Sagineedu, J. Stanslas and W. S. Wong, Andrographolide and its analogues: versatile bioactive molecules for combating inflammation and cancer, Clinical and Experimental Pharmacology & Physiology, Vol. 39, No. 3, pp. 300-310, 2012. DOI: 10.1111/j.1440-1681.2011.05633.x
- Mussard, A. Cesaro, E. Lespessailles, B. Legrain, S. Berteina-Raboin and H. Toumi, Andrographolide, a natural antioxidant: An update, Antioxidants (Basel), Vol. 8, No. 12, pp. 571, 2019. DOI: 10.3390/antiox8120571
- Patil, V. Jain, Andrographolide: A Review of analytical methods, Journal of Chromatographic science, Vol. 59, No. 2, pp. 191-203, 2021. DOI: 10.1093/chromsci/bmaa091
- Lu, Y. Ma et al., A review for the neuroprotective effects of andrographolide in the central nervous system, Biomed Pharmacother, Vol. 117, No. 109078, 2019. DOI: 10.1016/j.biopha.2019.109078
- Abedi et al., A review of the neuroprotective effects of andrographolide in Alzheimer's disease, Advances in Traditional Medicine, Vol. 21, pp. 253-266, 2021. DOI: 10.1007/s13596-021-00573-8
- J. Chan, W. S. Wong, P. T. Wong and J. S. Bian, Neuroprotective effects of andrographolide in a rat model of permanent cerebral ischaemia, Ritish Journal of Pharmacology, Vol. 161, No. 3, pp. 668-679, 2010. DOI: 10.1111/j.1476-5381.2010.00906.x
- K. Singha, S. Roy and S. Dey, Antimicrobial activity of andrographis paniculata, Fitoterapia, Vol. 74, No. 7-8, pp. 692-694, 2003. DOI: 10.1016/S0367-326X(03)00159-X
- T. Coon, E. Ernst, Andrographis paniculata in the treatment of upper respiratory tract infections: a systematic review of safety and efficacy, Planta Medica, Vol. 70, No. 4, pp. 293-298, 2004. DOI: 10.1055/s-2004-818938
- Y. Hu, R. H. Wu, M. Logue, C. Blondel and L. Y. Lai, Andrographis paniculata (Chuān Xīn Lián) for symptomatic relief of acute respiratory tract infections in adults and children: A systematic review and meta-analysis, PLoS One, Vol. 12, No. 8, e0181780, 2017. DOI: 10.1371/journal.pone.0181780
- Poolsup, C. Suthisisang, S. Prathanturarug, A. Asawamekin and U. Chanchareon, Andrographis paniculata in the symptomatic treatment of uncomplicated upper respiratory tract infection: systematic review of randomized controlled trials, Journal of Clinical Pharmacy and Therapeutics, Vol. 29, No. 1, pp. 37-45, 2004. DOI: 10.1046/j.1365-2710.2003.00534.x
- Hyung Ju Cho et al., Newly developed method for mouse olfactory behavior tests using an automatic video tracking system, Auris Nasus Larynx, Vol. 45, No. 1, pp. 103-110, 2018. DOI:10.1016/j.anl.2017.03.007
- Yang, J. N. Crawley, Simple behavioral assessment of mouse olfaction,Current protocols in neuroscience, Chapter 8, Unit-8.24, 2009. DOI: 10.1002/0471142301.ns0824s48
- B. Genter, D. M. Owens, H. B. Carlone and K. M. Crofton, Olfactory toxicity of methimazole: Dose-response and structure-activity studies and characterization of flavin-containing monooxygenase activity in the Long-Evans rat olfactory mucosa, Toxicologic Pathology, Vol. 23, No. 4, pp. 477-486, 1995. DOI: 10.1177/019262339502300404
- Sakamoto, K. Kondo, A. Kashio, K. Suzukawa and T. Yamasoba, Methimazole-induced cell death in rat olfactory receptor neurons occurs via apoptosis triggered through mitochondrial cytochrome c-mediated caspase-3 activation pathway, Journal of neuroscience research, Vol. 85, pp. 548-557, 2007. DOI: 10.1002/jnr.21155
- T. Huang, Y. Wei and Wu, Effects of olfactory training on posttraumatic olfactory dysfunction: a systematic review and meta-analysis, International forum of allergy & rhinology, Vol. 11, No. 7, pp. 1102-1112, 2021. DOI: 10.1002/alr.22758
- Worasuttayangkurn et al., Acute oral toxicity evaluation of Andrographis paniculata-standardized first true leaf ethanolic extract, Toxicology reports, Vol. 6, pp. 426-430, 2019.
- B. Brittebo, Metabolism-dependent toxicity of methimazole in the olfactory nasal mucosa, Pharmacology & toxicology, Vol. 76, No. 1, pp. 76-79, 1995. DOI: 10.1111/j.1600-0773.1995.tb00107.x
- P. Wang et al., Neuroprotective effects of andrographolide on chronic cerebral hypoperfusion-induced hippocampal neuronal damage in rats possibly via PTEN/AKT signaling pathway, Acta histochemica, Vol. 122, No. 3, pp. 151514, 2020. DOI: 10.1016/j.acthis.2020.151514
- Lee, A. M. Shen, M. Shah, O. B. Garbuzenko and T. Minko, In vivo evaluation of nose-to-brain delivery of liposomal donepezil, memantine, and BACE-1 siRNA for Alzheimer’s disease therapy, International Journal of Molecular Sciences, Vol. 25, No. 19, 10357, 2024. DOI: 10.3390/ijms251910357
- Yabuki, K. Matsuo, K. Hirano, Y. Shinoda, S. Moriguchi and K. Fukunaga, Combined memantine and donepezil treatment improves behavioral and psychological symptoms of dementia-like behaviors in olfactory bulbectomized mice, Pharmacology, Vol. 99, No. 3-4, pp. 160–171, 2017. DOI: 10.1159/000452839
- Yuan, A. Cheng, I. Kawahata, H. Izumi, J. Xu and K. Fukunaga, Single administration of the T-Type calcium channel enhancer SAK3 reduces oxidative Stress and improves cognition in olfactory bulbectomized mice, International Journal of Molecular Sciences, Vol. 22, No. 2, pp. 741, 2021. DOI: 10.3390/ijms22020741
- P. Mattson, Hormesis defined, Ageing Res Rev, Vol. 7, No. 1, pp. 1-7, 2008. DOI: 10.1016/j.arr.2007.08.007
- K. Mishra, N. S. Sangwan and R. S. Sangwan, Andrographis paniculata (Kalmegh): A review, Pharmacognosy Reviews, Vol. 1, No. 2, pp. 283-298, 2007.