Nghiên cứu hoạt tính sinh học và khả năng ứng dụng chiết xuất lá trầu không (Piper Betle L.) trong lớp phủ chống bám bẩn sinh học
Chi nhánh Ven Biển - Trung tâm Nhiệt đới Việt-Nga
Số điện thoại: 0869514226; Email: nda.ttndvn@gmail.com
Nội dung chính của bài viết
Tóm tắt
Bài báo này trình bày kết quả nghiên cứu khả năng sử dụng chiết xuất lá trầu không (Piper betle L.) với vai trò là một loại phụ gia kháng khuẩn cho lớp phủ chống bám bẩn sinh học thân thiện với môi trường. Hoạt chất sinh học của chiết xuất được xác định qua hàm lượng phenolic tổng số. Kết quả cho thấy hàm lượng phenolic tổng số trong chiết xuất đạt 260,3 mg GAE/g chất khô. Hoạt tính kháng khuẩn của chiết xuất được đánh giá bằng phương pháp khuếch tán trên đĩa thạch. Độc tính sinh học được đánh giá trên ấu trùng Artemia salina. Kết quả cho thấy, chiết xuất lá trầu không có hoạt tính kháng khuẩn cao đối với quần xã vi sinh vật biển với đường kính vòng kháng khuẩn đạt 35,1 ± 0,5 mm. Độc tính sinh học của chiết xuất đối với ấu trùng Artemia salina ở mức độ trung bình (LC50 > 100 µg/mL). Kết quả thử nghiệm tự nhiên trong môi trường nước biển trong điều kiện tĩnh cho thấy, việc bổ sung chiết xuất lá trầu không vào thành phần lớp phủ trên cơ sở acrylic copolymer giúp tăng đáng kể hiệu quả chống bám bẩn sinh học của lớp phủ. Tuy nhiên, ở điều kiện thử nghiệm động (thử nghiệm quay) hiệu quả chống bám bẩn của lớp phủ chứa chiết xuất thấp hơn đáng kể so với lớp phủ có sử dụng Cu2O
Abstract
Investigation of bioactivity and antifouling efficacy of Piper Betle L. extract in acrylic-based marine coatings
This study reports the potential use of Piper betle L. extract as an antibacterial additive for the development of environmentally friendly antifouling coatings. The bioactive potential of the extract was characterized through its total phenolic content, which was determined to be 260.3 mg GAE/g dry weight. Antibacterial activity was evaluated using the agar well diffusion method, while the biological toxicity was assessed on Artemia salina nauplii. The results revealed that the extract exhibited strong antibacterial activity against marine bacteria with an inhibition zone diameter of 35.1 ± 0.5 mm. Toxicity assessment on Artemia salina indicated that the extract can be classified as moderately toxic (LC₅₀ > 100 µg/mL). Field immersion tests under static seawater conditions demonstrated that the incorporation of Piper betle L. extract into an acrylic copolymer-based coating significantly enhanced its antifouling performance. However, under dynamic test conditions (rotating panel assay), the antifouling efficacy of the extract-containing coating was considerably lower compared to the coating formulated with Cu2O.
Từ khóa
hoạt tính kháng khuẩn, lớp phủ chống bám bẩn sinh học, hiệu quả chống bám bẩn sinh học, độc tính sinh học, Chiết xuất lá trầu không (Piper betle L.), Piper betle L. extract, antibacterial activity, antifouling coatings, antifouling efficiency, toxicity test
Chi tiết bài viết

Bài báo này được cấp phép theo Creative Commons Attribution 4.0 International License.
- Điểm nổi bật:
Trong thành phần chiết xuất lá trầu không (Piper betle L.) có chứa hàm lượng cao nhóm phenolic.
Chiết xuất lá trầu không có hoạt tính kháng khuẩn cao đối với quần xã vi sinh vật biển.
Chiết xuất có mức độ độc tính trung bình đối với ấu trùng Artemia salina.
Chứng minh hiệu quả chống bám bẩn sinh học khi bổ sung chiết xuất vào thành phần lớp phủ trên cơ sở acrylic copolymer.
1. ĐẶT VẤN ĐỀ
Trong bối cảnh các quy định về môi trường ngày càng nghiêm ngặt đối với việc sử dụng các loại sơn phủ chống bám bẩn chứa độc tố, nhu cầu phát triển các lớp phủ chống bám bẩn thân thiện với môi trường, sử dụng các phụ gia có nguồn gốc tự nhiên có độc tính thấp, ngày càng thu hút sự quan tâm của các nhà nghiên cứu [1]. Trong đó, một số hướng nghiên cứu có triển vọng là sử dụng các loại enzyme, chiết xuất từ các sinh vật biển (tảo, thân mềm, vi khuẩn biển…) và chiết xuất thực vật với vai trò là phụ gia chống bám bẩn [2].
So với enzyme và chiết xuất từ sinh vật biển, chiết xuất thực vật có nhiều ưu điểm như nguồn cung nguyên liệu dồi dào, chi phí thấp và quy trình chiết xuất đơn giản. Các chiết xuất này có thể thu được từ các bộ phận khác nhau của thực vật như rễ, vỏ, lá, quả… Chiết xuất thực vật có chứa hàm lượng cao các nhóm hợp chất polyphenol như phenolic, flavonoid, phenolic acid, polyphenolic amid [3]. Đây là các nhóm có hoạt tính kháng khuẩn cao, có tiềm năng ứng dụng trong ngành công nghiệp dược phẩm cũng như trong chế tạo các lớp phủ chống bám bẩn. Một số loại chiết xuất thực vật đã được nghiên cứu sử dụng với vai trò là phụ gia chống bám bẩn cho các lớp phủ có thể kể đến như: chiết xuất capsaicin từ quả ớt [4], chiết xuất củ gừng [5], củ nghệ [6], chiết xuất lá đước [7], chiết xuất cây keo đen [8]. Kết quả thử nghiệm tự nhiên trong môi trường nước biển cho thấy, lớp phủ sử dụng chiết xuất thực vật có hiệu quả chống bám bẩn khá cao trong thời gian thử nghiệm từ 6 - 9 tháng [4-8].
Trầu không (Piper betle) là loài thực vật phân bố phổ biến ở Việt Nam. Chiết xuất lá trầu không có hiệu quả kháng khuẩn cao, được sử dụng như là một loại thuốc đông y chữa các bệnh nhiễm khuẩn răng miệng. Trong thành phần của chiết xuất lá trầu không có chứa một số nhóm hợp chất như phenolic, tannin, alkaloid, saponin, flavonoid [9]. Các nghiên cứu cho thấy, chiết xuất lá trầu không có hoạt tính kháng khuẩn cao đối với các chủng vi khuẩn điển hình như E. coli, B. cereus, Salmonella sp. và Shigella sp. [10].
Trong nghiên cứu này, chúng tôi sử dụng chiết xuất lá trầu không với vai trò là phụ gia chống bám bẩn cho lớp phủ trên cơ sở acrylic copolymer với mục tiêu chế tạo lớp phủ chống bám bẩn thân thiện với môi trường, có hiệu quả chống bám bẩn cao, thay thế cho các lớp phủ chống bám bẩn chứa độc tố truyền thống.
2. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU
2.1. Vật liệu, hóa chất
Nguyên liệu chính sử dụng trong nghiên cứu bao gồm: lá trầu không (Piper betle L.) được sấy khô, nghiền mịn với kích thước ≤ 500 µm; ethanol (C2H5OH, độ tinh khiết ≥ 99,5%, Fisher Chemical, Hoa Kỳ); thuốc thử phenol Folin-Ciocalteu (Merck, Đức); acid gallic (≥ 99%, Sigma, Đức); môi trường nuôi cấy Marine Broth và Marine Agar (Himedia, Ấn Độ); nhựa acrylic copolymer B116 (Mitsubishi, Nhật Bản); ZnO (99,8%, Xilong, Trung Quốc); CaCO3 (99,8%, Xilong, Trung Quốc); betonite (≥ 99%, Xilong, Trung Quốc); xylene (C8H10, Xilong, Trung Quốc).
2.2. Thu chiết xuất lá trầu không
Lá trầu không (Piper betle L.) được thu tại Nha Trang, Khánh Hòa vào tháng 9 năm 2024. Sau đó, lá trầu được rửa sạch và sấy ở nhiệt độ 45oC trong khoảng 72 giờ. Nguyên liệu sau sấy được nghiền mịn bằng cối xay đến kích thước ≤ 500 µm. Bột lá trầu không (200 g) được ngâm trong dung môi ethanol với tỷ lệ bột:dung môi là 1:10 (g:mL) trong khoảng 24 giờ ở nhiệt độ phòng. Hỗn hợp sau chiết được lọc qua giấy lọc để loại bỏ cặn. Quá trình này lặp lại 3 lần để đảm bảo thu tối đa chất chiết. Sau đó, dịch chiết được cô đặc bằng máy cô quay chân không ở nhiệt độ 40oC, áp suất 175 mbar. Dịch chiết cô đặc được sấy trong tủ sấy chân không trong khoảng 48 giờ để loại bỏ hoàn toàn dung môi. Cao chiết cô đặc được bảo quản trong tủ mát ở nhiệt độ 4oC để phục vụ các bước nghiên cứu tiếp theo. Khối lượng cao chiết thu được là 28,40 g (hiệu suất thu cao chiết đạt 14,2%).
2.3. Nghiên cứu tính chất của chiết xuất
Thành phần các nhóm chức hữu cơ trong cao chiết được đánh giá bằng phương pháp phổ hồng ngoại biến đổi Fourier (FTIR) trong dải số sóng từ 4000 đến 630 cm-1 sử dụng thiết bị Agilent Cary 630 (Agilent Technologies, Malaysia).
Xác định hàm lượng phenolic tổng trong mẫu chiết xuất. Hút 0,5 mL dịch chiết (đã pha loãng bằng ethanol đến nồng độ 5 µg/mL) trộn với 2,5 mL thuốc thử Folin-Ciocalteu 10% (v/v) trong nước cất, để ổn định trong 6 phút. Sau đó, thêm vào 2 mL dung dịch Na2CO3 7,5% (w/v) trong nước cất và ủ trong bóng tối ở nhiệt độ phòng trong 1 giờ. Độ hấp thụ của hỗn hợp được đo ở 765 nm sử dụng máy quang phổ UV-Vis DR3900 (Hach, Đức). Acid gallic được sử dụng làm chất chuẩn. Hàm lượng phenolic tổng số được biểu diễn tương đương với mg GAE/g chất khô [11].
Đánh giá hoạt tính kháng khuẩn. Hoạt tính kháng khuẩn của chiết xuất lá trầu không được đánh giá đối với quần xã vi sinh vật biển bằng phương pháp khuếch tán trên đĩa thạch [12]. Mẫu nước biển được thu tại khu vực Phao thử nghiệm biển, Trạm nghiên cứu thử nghiệm biển Đầm Báy (Vịnh Nha Trang, 12o12’ N, 109°18’ E). Nuôi cấy tăng sinh trong môi trường Marine Broth ở điều kiện 32oC, lắc 150 vòng/phút trong thời gian 16 giờ. Trước khi tiến hành thử nghiệm, dịch nuôi cấy được pha loãng đến độ đục tương đương chuẩn McFarland 0,5 (1,5 x 108 CFU/mL). Chuẩn bị các đĩa thạch rắn Marine Agar. Hút 100 µL dịch vi khuẩn đã pha loãng, cấy trang đều lên bề mặt đĩa thạch. Dùng dụng cụ vô trùng đục các giếng thạch đường kính 6 mm, sau đó nhỏ vào mỗi giếng 70 µL dịch chiết lá trầu không (đã pha loãng bằng ethanol đến nồng độ 300 µg/mL). Ethanol được sử dụng làm đối chứng âm. Đối chứng dương là Penicillin G nồng độ 6 µg/mL. Các đĩa thạch được ủ trong 24 giờ ở 32oC. Hoạt tính kháng khuẩn được xác định bằng cách đo đường kính vòng kháng khuẩn (mm) quanh mỗi giếng thạch.
Đánh giá độc tính của chiết xuất đối với ấu trùng Artemia salina. Các mẫu được thử nghiệm ở điều kiện tĩnh trong khoảng thời gian 48 giờ ở nhiệt độ phòng trong đĩa petri thủy tinh đóng kín. Ấu trùng Artemia nở giai đoạn II – III được cho tiếp xúc với chiết xuất và độc chất so sánh ở các nồng độ khác nhau. Độc chất so sánh được sử dụng là polyhexamethylene guanidine (PHMG). Đánh giá mức độ tử vong của ấu trùng sau 48 giờ sử dụng kính hiển vi quang học. Để tính toán nồng độ gây tử vong bán phần (LC50) của từng loại hợp chất, chúng được thử từ nồng độ 500 µg/mL đến nồng độ mà ở đó không gây tử vong đối với ấu trùng Artemia salina. Sau đó dựng đồ thị phụ thuộc “Log nồng độ - tỷ lệ tử vong của ấu trùng”, dựa vào phương trình hồi quy để tính giá trị LC50 (nồng độ mà ở đó 50% số ấu trùng bị tử vong). Thí nghiệm được lặp lại 5 lần. Kết quả được biểu diễn dưới dạng giá trị trung bình ± độ lệch chuẩn.
2.4. Chế tạo và đánh giá tính chất của của lớp phủ
Chế tạo lớp phủ: Các mẫu sơn trên cơ sở acrylic copolymer được chế tạo theo công thức phối trộn như sau: 15 g copolymer, 10 g CaCO3, 10 g ZnO, 2 g betonite và 100 ml xylene (dung môi). Phụ gia chiết xuất được bổ sung vào thành phần sơn phủ với hàm lượng lần lượt là 0,5; 1,0 và 1,5% (theo khối lượng). Mẫu sơn không chứa phụ gia chiết xuất được sử dụng làm mẫu đối chứng. Các mẫu sơn được thi công bằng phương pháp phun trên nền thép Ct3. Chiều dày lớp phủ trung bình đạt 89 ± 3 µm.
Độ bám dính của lớp phủ được xác định bằng phương pháp kéo nhổ (pull-off) theo tiêu chuẩn ASTM D4541-22.
Xác định tốc độ tự mài mòn của lớp phủ. Nghiên cứu xác định tốc độ tự mài mòn của lớp phủ được tiến hành trong phòng thí nghiệm với thời gian thử nghiệm 10 ngày trong nước biển theo phương pháp được mô tả trong [13]. Theo đó, các mẫu lớp phủ kích thước 3 x 3 cm với thành phần khác nhau được cân khối lượng, sau đó đặt vào các lọ chứa 150 mL nước biển và được đặt trên máy lắc tròn Grant-bio PSU-20i với tốc độ 120 vòng/phút. Đối với mỗi loại lớp phủ tiến hành thử nghiệm 3 mẫu thử. Để xác định tốc độ tự mài mòn, các mẫu lớp phủ sau khi ngâm 10 ngày được để khô tự nhiên ở nhiệt độ phòng trong khoảng 48 giờ. Sau đó tiến hành cân mẫu bằng cân phân tích có độ chính xác đến 0,001 g. Tốc độ tự mài mòn được tính theo công thức:

Trong đó: V là tốc độ tự mài mòn của lớp phủ, mg/cm2.ngày; W0 - khối lượng mẫu trước khi ngâm; Wt.dry - khối lượng mẫu sau khi ngâm để khô; S - diện tích mẫu.
Thử nghiệm tự nhiên đánh giá hiệu quả chống bám bẩn. Các mẫu lớp phủ được thử nghiệm trong điều kiện nhúng hoàn toàn trong nước biển ở độ sâu từ 0,5 đến 1,5 m tại Trạm nghiên cứu thử nghiệm biển Đầm Báy (Vịnh Nha Trang, 12o12’ N, 109°18’ E). Thông số trung bình của nước biển tại địa điểm thử nghiệm: Nhiệt độ - 29,4oC; pH - 8,27; hàm lượng ôxy hòa tan - 6,47 g/mL; Độ mặn - 33,4‰. Tiến hành thử nghiệm ở cả hai điều kiện thử nghiệm tĩnh và thử nghiệm động (giá thử nghiệm quay). Đối với mỗi thành phần lớp phủ tiến hành thử nghiệm 3 mẫu. Mẫu lớp phủ không chứa phụ gia chiết xuất được sử dụng làm mẫu đối chứng âm. Mẫu lớp phủ chứa 20% Cu2O (theo khối lượng) được sử dụng làm mẫu đối chứng dương. Đối với điều kiện thử nghiệm tĩnh, các mẫu lớp phủ được cố định theo phương thẳng đứng trên các giá thử nghiệm sao cho khoảng cách tối thiểu giữa các mẫu không nhỏ hơn 10 cm, khoảng cách giữa các giá thử nghiệm không nhỏ hơn 20 cm. Đối với điều kiện thử nghiệm quay, các mẫu thử nghiệm được cố định trên giá thử nghiệm đặt trong lồng quay đường kính 2,2 m, tốc độ quay khoảng 3,6 m/s.
Đánh giá hiệu quả chống bám bẩn của các mẫu thử nghiệm được thực hiện theo phương pháp của Silva E. R. và cộng sự trong [14]. Theo đó, để đánh giá sơ bộ bám bẩn các mẫu thử nghiệm, các mẫu được nhấc lên khỏi mặt nước, chụp ảnh bề mặt mẫu. Tiếp theo, các mẫu được quan sát trên máy tính với độ phân giải cao và tính toán diện tích bám bẩn trên bề mặt mẫu sử dụng chương trình ImageJ 1.48v. Hiệu quả chống bám bẩn được tính theo loại sinh vật bám và diện tích bám bẩn theo công thức:
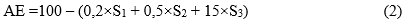
Trong đó: AE là hiệu quả chống bám bẩn của lớp phủ, %; S1 - phần trăm diện tích lớp phủ bị bám bẩn bởi màng vi sinh; S2 - phần trăm diện tích bề mặt lớp phủ bị bám bẩn bởi các loại sinh vật bám có kích thước nhỏ hơn 5 mm; S3 - phần trăm diện tích bề mặt bị bám bẩn bởi sinh vật bám có kích thước lớn hơn 5mm.
3. KẾT QUẢ VÀ THẢO LUẬN
3.1. Thành phần các hợp chất hữu cơ trong chiết xuất lá trầu không
Phổ hồng ngoại của chiết xuất lá trầu không được trình bày ở Hình 1. Có thể thấy, một dải hấp thụ rộng ở số sóng 3354 cm-1 phản ánh dao động hóa trị của liên kết O-H trong các nhóm carboxylic hoặc hydroxyl. Đỉnh hấp thụ ở số sóng 2922 cm-1 phản ánh dao động kéo giãn của liên kết C-H trong nhóm methyl trên vòng thơm. Đỉnh hấp thụ tại số sóng 1714 cm-1 đặc trưng cho dao động kéo giãn của liên kết C=O, có thể liên quan đến sự hiện diện của các hợp chất nhóm phenolic. Ngoài ra, đỉnh hấp thụ tại số sóng 1510 cm-1 đặc trưng cho dao động kéo giãn C=C trong vòng thơm [15].
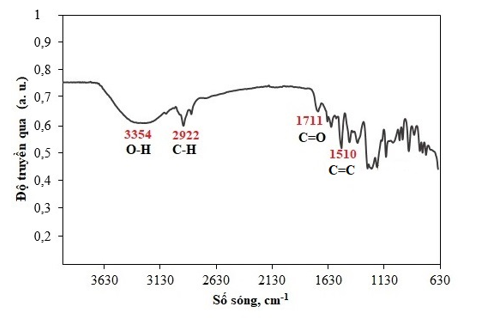
Hình 1. Phổ hồng ngoại của chiết xuất lá trầu không (Piper betle L.)
Kết quả phân tích hàm lượng phenolic tổng số cho thấy, trong thành phần của chiết xuất lá trầu không có chứa hàm lượng phenolic khá cao (260,3 mg GAE/g chất khô). Kết quả phân tích này cũng tương đồng với nghiên cứu khác về hàm lượng phenolic tổng số của chiết lá trầu không thu tại Nepal [16]. Trong khi đó, trong thành phần chiết xuất lá trầu không bằng phương pháp chiết siêu âm [17] có chứa hàm lượng phenolic cao hơn so với sử dụng phương pháp ngâm chiết trong dung môi. Tuy nhiên, phương pháp siêu âm thường đòi hỏi thiết bị chuyên dụng, chi phí cao và khó áp dụng ở quy mô lớn, trong khi phương pháp ngâm chiết đơn giản, tiết kiệm và dễ triển khai hơn trong thực tiễn sản xuất.
3.2. Hoạt tính kháng khuẩn và độc tính sinh học của chiết xuất lá trầu không
Để đánh giá khả năng sử dụng chiết xuất lá trầu không với vai trò phụ gia cho các lớp phủ chống bám bẩn, đã tiến hành nghiên cứu hoạt tính kháng khuẩn của chiết xuất đối với quần xã vi sinh vật biển và đánh giá độc tính sinh học đối với nhóm sinh vật không phải mục tiêu, sử dụng ấu trùng Artemia salina.
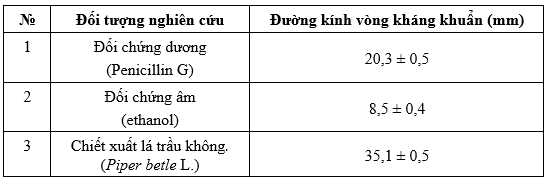
Kết quả đánh giá hoạt tính kháng khuẩn của chiết xuất lá trầu không được trình bày trong Bảng 1. Theo đó, chiết xuất bằng dung môi ethanol có hiệu quả kháng khuẩn cao đối với quần xã vi sinh vật biển với đường kính vòng kháng khuẩn đạt 35,1 ± 0,5 mm. So sánh với các nghiên cứu trước đó, chiết xuất ethanol của một số loài thực vật thu tại Malaysia có hoạt tính kháng khuẩn khá cao đối với chủng Pseudomonas spp. (một chủng vi sinh vật có trong thành phần của lớp màng bám bẩn sinh học) với đường kính vòng kháng khuẩn từ 9 đến 21 mm [18]. Chiết xuất ethanol từ các bộ phận khác nhau của quả ổi (Psidium guajava) cũng cho thấy hoạt tính kháng khuẩn đối với hai chủng vi khuẩn phổ biến trong thành phần màng bám bẩn là Pseudomonas spp. và Vibrio spp. với đường kính vòng kháng khuẩn trung bình lần lượt là khoảng 11,0 và 7,0 mm [19].
Bảng 1. Hoạt tính kháng khuẩn của chiết xuất lá trầu không (Piper betle L.) đối với quần xã vi sinh vật biển
Độc tính sinh học của chiết xuất được đánh giá đối với ấu trùng Artemia salina Sự phụ thuộc tỷ lệ tử vong của ấu trùng vào nồng độ của các hợp chất thử nghiệm được trình bày ở Hình 2. Có thể thấy, chiết xuất từ lá trầu không có độc tính sinh học thấp hơn nhiều so với chất diệt khuẩn PHMG. Đặc biệt, tỷ lệ tử vong của ấu trùng giảm nhanh khi nồng độ chiết xuất sử dụng dưới 100 µg/mL.
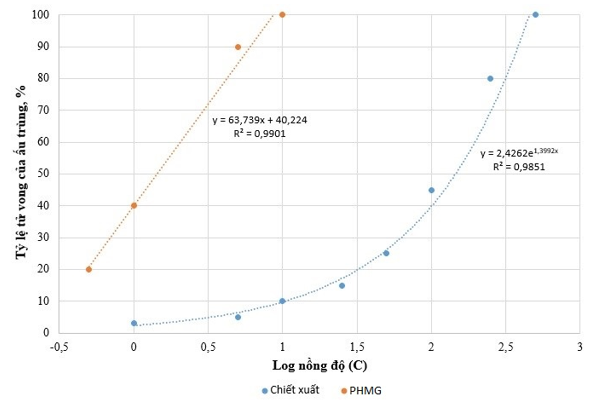
Hình 2. Đồ thị sự phụ thuộc của tỷ lệ tử vong của ấu trùng Artemia salina vào nồng độ hợp chất thử nghiệm
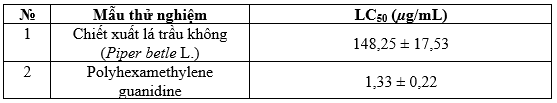
Kết quả ngoại suy giá trị nồng độ gây tử vong bán phần (LC50) của các loại hợp chất thử nghiệm được đưa ra ở Bảng 2. Kết quả cho thấy chiết xuất lá trầu không có tác dụng gây độc đối với ấu trùng Artemia salina với nồng độ LC50 là 148,25 ± 17,53µg/mL, trong khi đó hợp chất PHMG có nồng độ LC50 là 1,33 ± 0,22µg/mL. Theo bảng phân loại mức độ độc tính, PHMG được xếp vào nhóm có độc tính rất cao, còn chiết xuất từ lá trầu không được phân loại vào nhóm có độc tính trung bình.
Bảng 2. Giá trị nồng độ gây tử vong bán phần (LC50) ngoại suy từ Hình 2
3.3. Tính chất cơ học và hiệu quả chống bám bẩn của lớp phủ sử dụng chiết xuất lá trầu không
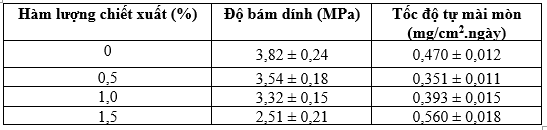
Kết quả xác định độ bám dính và tốc độ tự mài mòn của lớp phủ được trình bày ở Bảng 3. Có thể thấy, độ bám dính của lớp phủ giảm dần khi hàm lượng chiết xuất được bổ sung vào thành phần lớp phủ tăng lên. Đặc biệt, khi hàm lượng chiết xuất đạt 1,5%, độ bám dính của lớp phủ giảm rõ rệt, có thể là do sự hiện diện của các pha hữu cơ làm giảm mức độ tương thích giữa lớp phủ với nền kim loại. Đối với tốc độ tự mài mòn, giá trị này giảm khi lớp phủ chứa 0,5 và 1% chiết xuất, nhưng lại tăng lên khi hàm lượng chiết xuất đạt 1,5%. Kết quả này cho thấy, việc bổ sung chiết xuất lá trầu không với hàm lượng nhỏ có thể làm tăng tính ổn định của lớp phủ, có thể là do sự tương tác giữa các nhóm hợp chất hữu cơ trong chiết xuất với pha nền polymer, làm tăng liên kết nội tại, từ đó làm giảm quá trình tự mài mòn của lớp phủ. Tuy nhiên, khi hàm lượng chiết xuất tăng lên đến 1,5% nó có thể gây suy yếu liên kết cấu trúc polymer, gây ra sự tự mài mòn nhanh hơn.
Bảng 3. Giá trị độ bám dính và tốc độ tự mài mòn của lớp phủ chứa chiết xuất lá trầu không với các hàm lượng khác nhau
Từ kết quả nghiên cứu trên, để tối ưu hóa hiệu quả và chi phí, nhóm nghiên cứu quyết định lựa chọn lớp phủ chứa 1% chiết xuất để tiến hành thử nghiệm tự nhiên đánh giá hiệu quả chống bám bẩn. Các mẫu lớp phủ được đặt thử nghiệm trong nước biển tại Phao thử nghiệm biển Đầm Báy. Ảnh chụp bề mặt các mẫu lớp phủ sau 6 tháng thử nghiệm trong điều kiện thử nghiệm tĩnh và thử nghiệm động (trên giá thử nghiệm quay) được trình bày ở Hình 3.

Hình 3. Ảnh chụp bề mặt các mẫu lớp phủ trước và sau 6 tháng thử nghiệm tự nhiên trong nước biển tại Phao thử nghiệm biển Đầm Báy: a) thử nghiệm tĩnh; b) thử nghiệm quay
Kết quả cho thấy, sau 6 tháng thử nghiệm trong điều kiện thử nghiệm tĩnh, mẫu lớp phủ chứa 1% (về khối lượng) chiết xuất vẫn thể hiện khả năng chống bám bẩn khá cao. Trên bề mặt mẫu chỉ xuất hiện lớp bám bẩn mỏng từ rêu và tảo cát, chưa xuất hiện bám bẩn macro. Trong khi đó, trên bề mặt mẫu lớp phủ không chứa phụ gia đã xuất hiện bám bẩn macro ở cạnh bên phải của mẫu (Hình 3a). Ngược lại, trong điều kiện thử nghiệm động, chỉ có mẫu lớp phủ chứa độc tố Cu2O là còn duy trì được khả năng chống bám bẩn sau 6 tháng thử nghiệm. Các mẫu lớp phủ không chứa phụ gia và lớp phủ chứa chiết xuất đã xuất hiện các tổ hàu hà trên bề mặt mẫu chỉ sau 1 tháng thử nghiệm. Sau 6 tháng thử nghiệm, bám bẩn macro đã bao phủ phần lớn bề mặt mẫu (Hình 3b). Hiệu quả chống bám bẩn của các mẫu lớp phủ thử nghiệm được trình bày ở hình 4. Có thể thấy, ở điều kiện thử nghiệm tĩnh, lớp phủ chứa 1% chiết xuất đạt hiệu quả chống bám bẩn trên 80% sau 6 tháng thử nghiệm, gần tương đương với mẫu lớp phủ chứa 20% Cu2O - một chất diệt khuẩn thường dùng trong các lớp phủ thương mại (Hình 4a). Tuy nhiên, khi thử nghiệm ở điều kiện thử nghiệm quay, hiệu quả chống bám bẩn của lớp phủ chứa chiết xuất suy giảm nhanh chóng so với mẫu lớp phủ chứa Cu2O. Sau 6 tháng thử nghiệm, hiệu quả chống bám bẩn của lớp phủ giảm xuống chỉ còn khoảng 15%, tương đương với mẫu đối chứng không chứa phụ gia. Trong khi đó mẫu lớp phủ chứa Cu2O vẫn duy trì được hiệu quả chống bám bẩn trên 70% (Hình 4b).
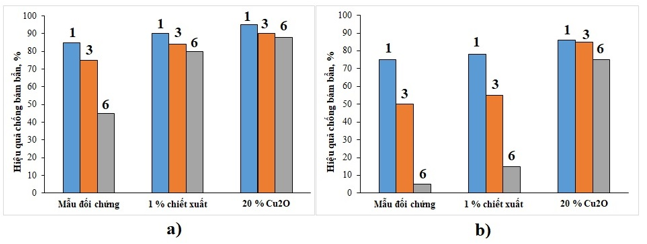
Hình 4. Hiệu quả chống bám bẩn của các lớp phủ sau 6 tháng thử nghiệm tự nhiên trong nước biển: a) thử nghiệm tĩnh; b) thử nghiệm quay
4. THẢO LUẬN
Trong thành phần của các chiết xuất thực vật, các hợp chất thuộc nhóm phenolic và flavonoid thường chiếm tỷ lệ cao và đóng vai trò quan trọng trong hoạt tính sinh học, đặc biệt là khả năng kháng khuẩn. Cần lưu ý rằng các hợp chất nhóm phenolic có trong chiết xuất lá trầu không được xác định là nhóm hợp chất đóng vai trò kháng khuẩn chính của chiết xuất [20, 21]. Một số hợp chất thuộc nhóm phenolic được tìm thấy trong chiết xuất lá trầu không có thể kể đến như: allyl pyrocatechol, allylcatechol, methyl eugenol, estragol (methyl chavicol), chavibetol, chavibetol acetate, safrol, 4-allyl-2-methoxy-phenolacetate và 3-allyl-6-methoxyphenol [22].
So với chiết xuất từ các loài thực vật khác, chiết xuất lá trầu không thể hiện hoạt tính kháng khuẩn cao đối với cả vi khuẩn Gram âm và Gram dương [23]. Trong đó, chiết xuất lá trầu không bằng dung môi ethanol cho hiệu quả kháng khuẩn cao nhất. Dịch chiết xuất lá trầu không trong dung môi ethanol nồng độ 50 - 100 µg/mL có hoạt tính kháng khuẩn cao nhất đối với các chủng vi khuẩn E. coli và P. aeruginosa [16]. Trong nghiên cứu [24], các tác giả cũng đã chỉ ra rằng, các hợp chất nhóm phenolic trong chiết xuất lá trầu không như hydroxychavicol và allylpyrocatechol, có khả năng ngăn chặn sự hình thành mảng bám trên răng bằng cách phá vỡ thành tế bào của vi khuẩn gây mảng bám S. sanguinis. Kết quả này đã thể hiện tiềm năng sử dụng chiết xuất lá trầu không để ngăn ngừa và loại bỏ bám bẩn thông qua việc ức chế sự phát triển và tiêu diệt vi sinh vật bám. Kết quả thử nghiệm kháng khuẩn trong nghiên cứu này cũng chứng minh chiết xuất lá trầu không có hoạt tính kháng khuẩn cao đối với vi sinh vật biển và có tiềm năng sử dụng như là một loại hoạt chất kháng khuẩn cho lớp phủ chống bám bẩn. Ngoài ra, các thử nghiệm độc tính cho thấy, chiết xuất từ thực vật thường có độc tính đối với ấu trùng Artemia salina ở mức từ trung bình đến thấp [25, 26]. Trong khi đó, các loại độc tố tổng hợp sử dụng trong thành phần của các lớp phủ chống bám bẩn thường có độc tính rất cao, với nồng độ LC50 < 5 µg/mL [27]. Do đó, việc nghiên cứu thử nghiệm chiết xuất từ thực vật với vai trò là phụ gia kháng khuẩn cho các lớp phủ chống bám bẩn nhằm thay thế cho các loại phụ gia diệt khuẩn truyền thống sẽ giúp hạn chế tác động tiêu cực đến hệ sinh thái biển, hướng đến các giải pháp bền vững và thân thiện với môi trường.
Kết quả thử nghiệm tự nhiên cho thấy, lớp phủ chứa chiết xuất lá trầu không thể hiện hiệu quả chống bám bẩn cao ở điều kiện thử nghiệm tĩnh. Tuy nhiên, hiệu quả này suy giảm nhanh chóng trong điều kiện thử nghiệm động. Nguyên nhân chủ yếu có thể là do sự gia tăng tốc độ rửa trôi chiết xuất khỏi bề mặt lớp phủ dưới tác động của chuyển động, dẫn đến nồng độ hoạt chất trên bề mặt không duy trì đủ để ức chế sự phát triển của vi sinh vật bám. Bên cạnh đó, chiết xuất giải phóng bị pha loãng nhanh chóng dưới tác động của dòng chảy càng làm giảm hiệu quả chống bám bẩn của lớp phủ. Ngoài ra, khi thử nghiệm ở điều kiện thử nghiệm động, xác suất bắt gặp ấu trùng hàu hà và các sinh vật bám khác, trôi lơ lửng trong nước biển, cũng tăng lên đáng kể. Đồng thời, chuyển động của nước còn làm tăng lượng oxi hòa tan, tạo điều kiện thuận lợi cho sự phát triển của sinh vật bám.
Một trong những hạn chế chính của các lớp phủ chống bám bẩn sử dụng chiết xuất sinh học từ thực vật là khó duy trì hiệu quả chống bám bẩn ổn định trong thời gian dài. Điều này xuất phát từ thách thức trong việc kiểm soát tốc độ giải phóng hoạt chất khỏi bề mặt lớp phủ. Để giải quyết vấn đề này, hiện nay các nghiên cứu đang tập trung vào một số hướng như: đóng gói chiết xuất vào các vi nang (micro capsule) [28] hoặc biến tính lớp phủ để kiểm soát tốc độ giải phóng hoạt chất [29].
5. KẾT LUẬN
Trong nghiên cứu này, chiết xuất lá trầu không (Piper betle L.) trong dung môi ethanol được thu nhận, đánh giá hoạt tính sinh học và hiệu quả chống bám bẩn khi sử dụng như là một loại phụ gia kháng khuẩn cho các lớp phủ chống bám bẩn sinh học. Kết quả cho thấy, trong thành phần của chiết xuất lá trầu không có chứa hàm lượng phenolic tổng số cao (260,3 mg GAE/g chất khô). Chiết xuất thể hiện hoạt tính kháng khuẩn cao đối với quần xã vi sinh vật biển, đồng thời có độc tính sinh học thấp đối với ấu trùng Artemia salina. Hiệu quả chống bám bẩn của lớp phủ trên cơ sở acrylic copolymer chứa chiết xuất lá trầu không với hàm lượng 1% (về khối lượng) đạt trên 80% sau 6 tháng thử nghiệm trong môi trường nước biển nhiệt đới ở điều kiện thử nghiệm tĩnh. Tuy nhiên, ở điều kiện thử nghiệm động (thử nghiệm quay) hiệu quả chống bám bẩn của lớp phủ chứa chiết xuất thấp hơn đáng kể so với lớp phủ có sử dụng Cu2O. Để tăng cường hiệu quả chống bám bẩn của lớp phủ, nghiên cứu có thể mở rộng theo hướng đóng gói chiết xuất vào các vi nang nhằm kiểm soát tốc độ giải phóng hoạt chất khỏi bề mặt lớp phủ.
Lời cảm ơn: Các tác giả xin gửi lời cảm ơn đến Chi nhánh Ven Biển, Trung tâm Nhiệt đới Việt-Nga đã tạo điều kiện thuận lợi về vật tư và trang thiết bị phục vụ nghiên cứu.
Tuyên bố về sử dụng Gen AI: Các công cụ AI tạo sinh không được sử dụng để tạo ra hoặc chỉnh sửa nội dung khoa học của bản thảo này. Trong phần có sử dụng công cụ AI (chỉ hỗ trợ kiểm tra ngữ pháp/định dạng), các tác giả đã kiểm tra toàn bộ nội dung và hoàn toàn chịu trách nhiệm đối với nội dung cuối cùng.
Tuyên bố về đóng góp của tác giả: Nguyễn Đức Anh: thu chiết xuất, bố trí thí nghiệm, chế tạo lớp phủ, tổng quan và viết bản thảo bài báo; Cao Nhật Linh: tổng quan và viết bản thảo bài báo, thảo luận kết quả; Lê Thị Mỹ Hiệp, Nguyễn Thị Hồng Xanh: thực hiện các thí nghiệm đánh giá hoạt tính kháng khuẩn và độc tính sinh học; Đồng Văn Kiên: Chế tạo lớp phủ, đánh giá mẫu lớp phủ thử nghiệm tự nhiên.
Tuyên bố về xung đột lợi ích: Các tác giả tuyên bố không có xung đột lợi ích.
Tài liệu tham khảo
- K. Kyei, G. Darko and O. Akaranta, Chemistry and application of emerging ecofriendly antifouling paints: A review, Journal of Coatings Technology and Research, Vol. 17, pp. 315–332, 2020. DOI: 10.1007/s11998-019-00294-3
- Chen et al., Biomimetic surface coatings for marine antifouling: Natural antifoulants, synthetic polymers and surface microtopography, Science of The Total Environment, Vol. 766, pp. 144469, 2021. DOI: 10.1016/j.scitotenv.2020.144469
- B. Rashmi, P. S. Negi, Chapter 3. Chemistry of plant extracts, in Plant Extracts: Applications in the Food Industry, Elsevier, 2022, pp. 39-73. DOI: 10.1016/B978-0-12-822475-5.00004-1
- An, X. Yang, W. Dong, C. Ni and X. Jiang, Synthesis and fouling resistance of capsaicin derivatives containing amide groups, Chemical Physics Letters, Vol. 808, pp. 139824, 2022. DOI: 10.1016/j.scitotenv.2019.136361
- Etoh et al., Shogaols from Zingiber ocinale as Promising Antifouling Agents, Bioscience, Biotechnology, and Biochemistry, Vol. 66, No. 8, pp. 1748–1750, 2002. DOI: 10.1271/bbb.66.1748
- Deng et al., Development of a curcumin-based antifouling and anticorrosion sustainable polybenzoxazine resin composite coating, Composites Part B: Engineering, Vol. 225, pp. 109263, 2021. DOI: 10.1016/j.compositesb.2021.109263
- Feng, W. Wang, X. Wang, Y. Qiu and C. Ke, Low barnacle fouling on leaves of the mangrove plant Sonneratia apetala and possible anti-barnacle defense strategies, Marine Ecology Progress Series, Vol. 554, pp. 169-182, 2016. DOI: 10.3354/meps11585
- S. Peres, E. Armelin, C. Aleman and C.A. Ferreira, Modified tannin extracted from black wattle tree as an environmentally friendly antifouling pigment, Industrial Crops and Products, Vol. 65, pp. 506–514, 2015. DOI: 10.1016/j.indcrop.2014.10.033
- Lam Thi Truc Nguyen, Thuong Thi Nguyen, Hoa Ngoc Nguyen and Quynh Thi Phuong Bui, Simultaneous determination of active compounds in Piper betle Linn. leaf extract and effect of extracting solvents on bioactivity, Engineering Reports, Vol. 2, pp. e12246, 2020. DOI:10.1002/eng2.12246
- Nhu Ngoc Nguyen, Nguyet Minh Vu Thi, Tuyen Phung Thi and Huong Lan Nguyen Thi, Antibacterial and antifungal activities of the ethanol extract of some medicinal plants, Vietnamese Journal of Food Control, Vol. 3, No. 4, pp. 261-269, 2020. DOI: 10.47866/2615-9252/vjfc.1760
- L. Singleton, R. Orthofer and M. Lamuela-Raventós Rosa, Analysis of total phenols and other oxidation substrates and an-tioxidants by means of folin-ciocalteu reagent, Methods in Enzymology, Vol. 299, pp. 152-178, 1999. DOI: 10.1016/S0076-6879(99)99017-1
- Kharchenko et al. Antifouling efficiency of polymer coatings with SeNPs-loaded SiO2(rh)-PHMG composite as antimicrobial agent, Journal of Coatings Technology and Research, Vol. 21, pp. 1467-1482, 2024. DOI: 10.1007/s11998-023-00907-y
- Wang, J. Xu, J. Yang and S. Zhou, Preparation and synergistic antifouling effect of self-renewable coatings containing quaternary ammonium-functionalized SiO2 nanoparticles, Journal of Colloid and Interface Science, Vol. 563, pp. 261-271, 2020. DOI: 10.1016/j.jcis.2019.12.086
- R. Silva et al., Eco-friendly non-biocide-release coatings for marine biofouling prevention, Science of The Total Environment, Vol. 650, No. 2, pp. 2499-2511, 2019. DOI: 10.1016/j.scitotenv.2018.10.010
- Б. Н. Тарасевич, ИК спектры основных классов органических соединений, Справочные материалы, Москва, Изд. МГУ, 2012, 52 с.
- Kaveti, L. Tan, T. S. Kuan and M. Baig, Antibacterial Activity Of Piper Betel Leaves, International Journal of Pharmacy Teaching and Practices, Vol. 2, No. 3, pp. 129-132, 2011
- Hoàng Thùy Dương et al., Đánh giá hoạt tính sinh học của cao chiết lá trầu không (Piper betle L.) thu nhận bằng phương pháp chiết siêu âm, Tạp chí Khoa học Kỹ thuật và Công nghệ, số 64(3), tr. 37-42, 2022. DOI: 10.31276/VJST.64(3).37-42
- M. Bahurmiz, R. Ahmad, N. Ismail, F. Adzitey and S. F. Sulaiman, Antimicrobial activity of various plant extracts on Pseudomonas species associated with spoilage of chilled fish, Turkish Journal of Agriculture - Food Science and Technology, Vol. 4, No. 11, pp. 1017-1023, 2016. DOI: 10.24925/turjaf.v4i11.1017-1023.668
- Tahera, F. Feroz, J. D. Senjuti, K. K. Das and R. Noor, Demonstration of anti-bacterial activity of commonly available fruit extracts in Dhaka, Bangladesh, American Journal of Microbiological Research, Vol. 2, No. 2, pp. 68-73, 2014. DOI: 10.12691/ajmr-2-2-5
- Taukoorah, N. Lall and F. Mahomoodally, Piper betle L. (betel quid) shows bacteriostatic, additive, and synergistic antimi-crobial action when combined with conventional antibiotics, South African Journal of Botany, Vol. 105, pp. 133-140, 2016. DOI: 10.1016/j.sajb.2016.01.006
- P. Tan, E. W. C. Chan, Antioxidant, antityrosinase and antibacterial properties of fresh and processed leaves of Anacardium occidentale and Piper betle, Food Bioscience, Vol. 6, pp. 17-23, 2014. DOI: 10.1016/j.fbio.2014.03.001
- M.D.M.W. Nayaka et al., Piper betle L.: recent review of antibacterial and antifungal properties, safety profiles, and commercial applications, Molecules, Vol. 26, No. 8, pp. 2321, 2021. DOI: 10.3390/molecules26082321
- Teanpaisan, P. Kawsud, N. Pahumunto and J. Puripattanavong, Screening for antibacterial and antibiofilm activity in Thai medicinal plant extracts against oral microorganisms, Journal of Tradiional and Complementary Medicine, Vol. 7, No. 2, pp. 172–177, 2016. DOI: 10.1016/j.jtcme.2016.06.007
- Kurnia, G.S. Hutabarat, D. Windaryanti, T. Herlina, Y. Herdiyati and M. H. Satari, Potential allylpyrocatechol derivatives as antibacterial agent against oral pathogen of S. Sanguinis ATCC 10,556 and as inhibitor of MurA Enzymes: In vitro and in silico study, Drug Design, Development and Therapy, Vol. 14, pp. 2977–2985, 2020. DOI: 10.2147/DDDT.S255269
- Nguyen Chi Mai, Nguyen Tuong Van, Pham Thi Hoe, Vu Huong Giang, Ninh Khac Ban and Tran My Linh, Optimization of brine shrimp lethality test for in vivo toxicity evaluation of poisonous plant species collected from Quang Tri province, Academia Journal of Biology, Vol. 46, No. 1, pp. 55-67, 2024. DOI: 10.15625/2615-9023/18899
- M. Karchesy, R. G. Kelsey, G. Constatine and J. J. Karchesy, Biological screening of selected Pacific Northwest forest plants using the brine shrimp (Artemia salina) toxicity bioassay, Springer Plus, Vol. 5, pp. 510, 2016. DOI: 10.1186/s40064-016-2145-1
- Panagoula, M. Panayiota and J. Iliopoulou-Georgudaki, Acute toxicity of TBT and IRGAROL in Artemia salina, International Journal of Toxicology, Vol. 21, No. 3, pp. 231-233, 2002. DOI:10.1080/10915810290096360
- Li, G. Wang, Z. Guo, P. Wang and A. Wang, Preparation of microcapsules coating and the study of their bionic anti-fouling performance, Materials, Vol. 13, No. 7, pp. 1669, 2020. DOI: 10.3390/ma13071669
- Lu et al., Flexible hydrophobic antifouling coating with oriented nanotopography and nonleaking capsaicin, ACS Applied Materials and Interfaces, Vol. 10, No. 11, pp. 9718–9726, 2018. DOI: 10.1021/acsami.7b19436